题目内容
8.(1)A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应的化学方程式,其中A,B的物质的量之比为1:4.请回答:①若Y是黄绿色气体,则该反应的离子方程式是MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;将Y与等物质的量的SO2充分混合后通入品红溶液,未见其褪色,原因是SO2+Cl2+2H2O=H2SO4+2HCl(请用化学方程式解释说明).
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应所得的氧化产物的化学式为CO2,反应中氧化剂与还原剂的物质的量之比是4:1
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,而且A可溶于X溶液中.
①A元素的元素符号为Fe,则A与B的反应中氧化剂与还原剂的物质的量之比是1:1.
②若含amol X的溶液溶解了一定量A后,此时溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量为0.4amol(用含a代数式表示);为保证A与B充分反应后最终所得的溶液中同时含有上述两种金属阳离子,则此时B与A的物质的量应满足的取值范围是$\frac{8}{3}$<n(B):n(A)<4.
分析 (1)若Y是黄绿色气体为Cl2,A、B的物质的量之比为1:4,应是二氧化锰与浓盐酸制备氯气,将Y为Cl2与等物的量的SO2充分混合后通入品红溶液氯气和二氧化硫恰好完全反应生成硫酸和氯化氢;
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,判断为C,B的溶液为浓硫酸,应是碳与浓硝酸反应,化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,氧化产物为CO2;根据电子得失守恒判断反应中氧化剂与还原剂的物质的量之比;
(3)A为金属单质,常温下A在B的浓溶液中“钝化”,则A为铁或铝,B为浓硫酸或浓硝酸,又A可溶于X溶液中则A为铁,由A、B的物质的量之比为1:4,该反应为铁与稀硝酸反应生成硝酸铁、一氧化氮和水;为保证A与B充分反应后最终所得的溶液中同时含有上述两种金属阳离子,可以依据极值计算分析判断.
解答 解:(1)若Y是黄绿色气体为Cl2,A、B的物质的量之比为1:4,应是二氧化锰与浓盐酸制备氯气,反应离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;将Y为Cl2与等物的量的SO2充分混合后通入品红溶液氯气和二氧化硫恰好完全反应生成硫酸和氯化氢,SO2+Cl2+2H2O=H2SO4+2HCl;
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,SO2+Cl2+2H2O=H2SO4+2HCl;
(2)若A为非金属单质,B的溶液为浓硫酸,应是碳与浓硝酸反应,化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,氧化产物为CO2,由化合价可知碳元素的化合价升高,则碳作还原剂,硝酸中氮元素的化合价降低,则硝酸作氧化剂,由化学计量数可知氧化剂与还原剂的物质的量之比为4:1,
故答案为:CO2;4:1;
(3)A为金属单质,常温下A在B的浓溶液中“钝化”,则A为铁或铝,B为浓硫酸或浓硝酸,又A可溶于X溶液中则A为铁,由A、B的物质的量之比为1:4,该反应为铁与稀硝酸反应生成硝酸铁、一氧化氮和水;
①铁为26号元素,元素符号为Fe,由A、B的物质的量之比为1:4,该反应为铁与稀硝酸反应生成硝酸铁、一氧化氮和水,Fe+4HNO3=Fe(NO3)3+NO↑+2H20,A与B的反应中氧化剂与还原剂的物质的量之比为1:1;
故答案为:Fe,1:1;
②设被还原的硝酸铁的物质的量为x,则:
2Fe3++Fe═3Fe2+,
2 3
x 1.5x
由溶液中两种金属阳离子的物质的量恰好相等,则a-x=1.5x,解得x=0.4a,
为保证A与B充分反应后最终所得的溶液中同时含有上述两种金属阳离子,可以依据极值计算分析判断取值
Fe+4HNO3=Fe(NO3)3+NO↑+2H20,
1 4
3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
3 8
则此时B与A的物质的量比应满足的取值范围是:$\frac{8}{3}$<n(B):n(A)<4,
故答案为:0.4a;$\frac{8}{3}$;4.
点评 本题较难,考查知识点较多,学生应熟悉常见的氧化还原反应及常见物质的性质是解答本题的关键,并能利用离子方程式或化学反应方程式来分析解答问题.

Ⅰ.AgNO3的热稳定性
利用如图所示的实验装置,加热A 中的AgNO3同体,试管A中有红棕色气体产生,B中无红棕色气体产生,在装置C中收集到无色气体.当反应结束后,测得试管中残留黑色同体Ag.(夹持及加热仪器均省略)
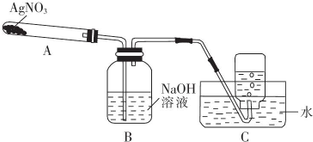
(1)如何检验整套装置的气密性?
(2)C中集气瓶收集的气体为氧气,要收集纯净的该气体,正确的操作是等到导气管中气泡均匀放出时再收集.
(3)AgNO3分解的化学方程式为2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑.
Ⅱ.AgNO3的氧化性
将光亮的铁丝伸入盛有AgNO3 溶液的大试管中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,
猜测如下:
假设一:Fe被氧化成Fe2+;
假设二:Fe被氧化成Fe3+;
假设三:Fe被氧化成Fe2+ 和Fe3+.
已知:溶液中的Ag+能与SCN-反应,干扰实验.选用如下试剂设计一个实验验证假设三.
可选用的试剂:KSCN溶液、酸性 KMnO4溶液、氯水、盐酸、硝酸、NaCl溶液.
请完成下表:
| 操作 | 现象 | 结论或目的 |
| (1)取少量溶液于试管中,向溶液中加入足量NaCl溶液 | - | 除尽Ag+ |
| (2)取少量上述溶液于试管中,加入KSCN溶液,振荡 | 溶液变血红色 | 存在Fe3+ |
| (3)取(1)中少量上述溶液于试管中,加入酸性KMnO4溶液,振荡 | 血红色消失 | 存在Fe2+ |
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 二氧化碳 | 一氧化碳 | 点燃 |
| B | 铁粉 | 铜粉 | 过量稀硫酸溶液、过滤 |
| C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D | 一氧化碳 | 二氧化碳 | 通过足量灼热的氧化铜 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
①用水鉴别苯、乙醇、溴苯;
②用饱和Na2CO3溶液鉴别乙酸、乙酸乙酯和CCl4;
③用酸性高锰酸钾鉴别正戊烷、己烯;
④用点燃的方法鉴别甲烷、乙烯.
| A. | ①② | B. | ①②④ | C. | ①③④ | D. | ①②③④ |
| A. | 标准状况下,18gD2O中所含的电子数为10NA | |
| B. | 200mL0.5mol•L-1的Na2CO3溶液中,由于CO32-水解,所以阴离子数目小于0.1NA | |
| C. | 精炼铜时,当阳极质量减少6.4g时,电路中转移电子数不一定为0.2NA | |
| D. | 5.6g铁与足量稀硫酸反应失去电子数为0.3NA |
( )
| A. | 反应中化合价升高的元素是NH3中的H | |
| B. | 该反应利用了Cl2的强还原性 | |
| C. | NH3在反应中得到电子 | |
| D. | 生成1molN2有6mol电子转移 |
 A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“--”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成.
A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“--”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成.