题目内容
15.下列变化中,符合周期表中同一周期主族元素从左到右递变规律的是( )| A. | 原子序数依次增加 | B. | 原子核外电子层数依次增加 | ||
| C. | 原子得电子能力逐渐减弱 | D. | 金属性逐渐增加 |
分析 根据同周期主族元素从左到右,电子层数不变,元素原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强,由此分析解答.
解答 解:A、同周期主族元素从左到右,电子层数不变,原子序数依次增加,故A正确;
B、同周期主族元素从左到右,电子层数不变,故B错误;
C、非金属性增加,元素原子得电子能力逐渐增加,故C错误;
D、同周期主族元素从左到右,电子层数不变,元素原子半径逐渐减小,非金属性逐渐增强,金属性减弱,故D错误;
故选:A.
点评 本题考查元素周期律的递变规律,题目难度不大,注意把握元素周期律的递变规律与元素在周期表中的位置关系.

练习册系列答案
相关题目
5.下列说法错误的是( )
| A. | 分子式为C4H8的烯烃有4种同分异构体,它们的熔点、沸点各不相同 | |
| B. | 乙烯、苯酚、乙醛均能与溴水反应,其反应原理各不相同 | |
| C. | 导电高分子材料PPV: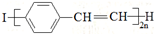 和聚苯乙烯具有相同的重复结构单元 和聚苯乙烯具有相同的重复结构单元 | |
| D. | 以淀粉为基本原料可制取乙酸乙酯 |
6.下列各组混合物,不能用分液漏斗分开的是( )
①四氯化碳、水 ②乙醇、甘油 ③乙醇、水 ④苯、水 ⑤已烷、水 ⑥环已烷、苯 ⑦溴苯、水.
①四氯化碳、水 ②乙醇、甘油 ③乙醇、水 ④苯、水 ⑤已烷、水 ⑥环已烷、苯 ⑦溴苯、水.
| A. | ②③⑥ | B. | ②④⑦ | C. | ①④⑤⑦ | D. | ③④⑥⑦ |
3.下列说法正确的是( )
| A. | 甲烷和乙醇均能发生取代反应 | |
| B. | 蛋白质、淀粉、油脂均能发生水解反应 | |
| C. | 溴乙烷与NaOH水溶液共热生成乙烯 | |
| D. | 油脂和淀粉都是高分子化合物 |
10.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 1.0mol/L 的Na2CO3溶液中:c(H+)+c(Na+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | 1.0mol/LNH4Cl溶液:c(NH4+)=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
7.能在空气中稳定存在的是( )
| A. | H2S水溶液 | B. | Na2SO3晶体 | C. | 漂白粉 | D. | Na2SO4晶体 |
4.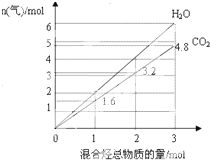 由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )
由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )
 由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )
由两种气态烃组成的混合物的总物质的量与该混合物充分燃烧后所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示,则以下对其组成的判断不正确的是( )| A. | 可能有乙烯 | B. | 一定有甲烷 | C. | 可能有丙烷 | D. | 一定没有丙烯 |
5.在标准状况下,将NO2、NO、O2混合并充满容器,然后把容器倒置于水槽中,充分反应后,水充满容器,则容器内HNO3的物质的量浓度的大小范围是( )
| A. | $\frac{1}{28}$<c(HNO3)<$\frac{1}{22.4}$ | B. | $\frac{1}{39.2}$<c(HNO3)<$\frac{1}{22.4}$ | ||
| C. | $\frac{1}{39.2}$<c(HNO3)<$\frac{1}{28}$ | D. | $\frac{1}{44.8}$<c(HNO3)<$\frac{1}{22.4}$ |