题目内容
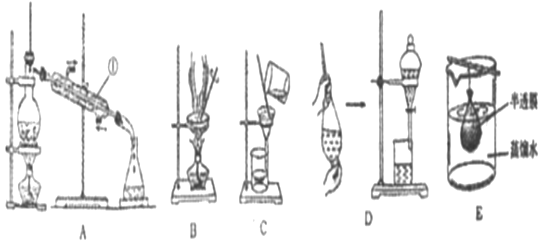
【题目】某同学设计下列方案对A盐的水解液进行鉴定:![]() 由此得出的结论中,不正确的是
由此得出的结论中,不正确的是
A. D溶液中存在Fe(SCN)3 B. A一定为无氧酸盐FeBr2 C. B为AgBr D. 滤液中有Fe3+
【答案】B
【解析】
由图中转化可以知道,B为A与硝酸银反应生成的浅黄色沉淀,根据元素守恒知则B为AgBr,所以A中含有Br-,C中加KSCN溶液变为血红色溶液,所以D为Fe(SCN)3溶液,则C中含有Fe3+,A中含有铁元素,硝酸具有强氧化性,能氧化亚铁离子生成铁离子,所以A为可能含有Fe3+或Fe2+。
A、通过以上分析知,D中含有Fe(SCN)3,故A正确;
B、硝酸具有强氧化性,能将亚铁离子氧化生成铁离子,所以A中可能是FeBr2,也可能是FeBr3,也可能是二者的混合物,故B错误;
C、B为A与硝酸银反应生成的浅黄色沉淀,根据元素守恒知则B为AgBr,故C正确;
D、能和硫氰化钾溶液反应生成血红色溶液,说明C中含有Fe3+,故D正确。
综上所述,本题选B。

练习册系列答案
相关题目