题目内容
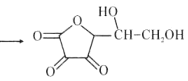
【题目】天门冬氨酸锌是一种补锌剂,可以用![]() 、天门冬氨酸为原料制备。
、天门冬氨酸为原料制备。
(1)![]() 基态核外电子排布式为_______。
基态核外电子排布式为_______。
(2)![]() 的空间构型为________(用文字描述);与
的空间构型为________(用文字描述);与![]() 互为等电子体的一种阳离子的化学式为________。
互为等电子体的一种阳离子的化学式为________。
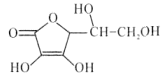
(3)天门冬氨酸( )分子中氮原子的轨道杂化类型为________;天门冬氨酸_______(填“难溶”或“易溶”)于
)分子中氮原子的轨道杂化类型为________;天门冬氨酸_______(填“难溶”或“易溶”)于![]() 盐酸。
盐酸。
(4)ZnO的晶胞结构如图所示,![]() 的配位数为________。
的配位数为________。

【答案】![]() 平面(正)三角形
平面(正)三角形 ![]()
![]() 易溶 4
易溶 4
【解析】
(1)Zn的基态核外电子排布式为![]() ,Zn失去最外层2个电子后,其核外电子排布式为:
,Zn失去最外层2个电子后,其核外电子排布式为:![]() ;
;
(2)![]() 中价层电子对数为:
中价层电子对数为:![]() =3,其化学键与O原子相连,其孤电子对数为0,其空间构型为平面三角形;H2O中价层电子总数为8+2=10,原子数为3,因此与H2O互为等电子体的一种阳离子为:
=3,其化学键与O原子相连,其孤电子对数为0,其空间构型为平面三角形;H2O中价层电子总数为8+2=10,原子数为3,因此与H2O互为等电子体的一种阳离子为:![]() ;
;
(3)N原子相连的δ键数为3,其价层电子对数为![]() =4,其轨道杂化类型为sp3;天门冬氨酸中含有亲水基(羧基、氨基),且氨基具有碱性,能与盐酸反应,因此天门冬氨酸易溶于盐酸;
=4,其轨道杂化类型为sp3;天门冬氨酸中含有亲水基(羧基、氨基),且氨基具有碱性,能与盐酸反应,因此天门冬氨酸易溶于盐酸;
(4)由图可知,与Zn2+相连的等距且距离最短的O2-有4个,因此Zn2+的配位数为4。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目