题目内容
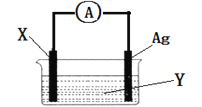
【题目】草酸晶体(H2C2O4·xH2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解,草酸钙难溶于水。某研究性小组按照下图装置,检验草酸晶体的分解产物中含有CO、CO2。已知C、E、H中盛装澄清石灰水,D中盛装浓NaOH溶液,G中盛有CuO。

(1)装置B的主要作用是_______。
(2)装置C中反应的离子方程式为_______。
(3)装置D的作用是_______。
(4)装置F所盛的药品是_______。
(5)能证明草酸晶体分解产物中有CO的现象是_______。
(6)H后连接的尾气处理装置为_______。(从“Ⅰ”“Ⅱ”中选择)
(7)为测定草酸晶体分子式(H2C2O4·xH2O) 中x的值,现做如下实验。
①称取6.3 g草酸晶体,将其配置成100.0 mL水溶液为待测溶液;
②取25.0 mL待测溶液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为0.4 mol/L的KMnO4标准溶液进行滴定,达到滴定终点时,用去12.50 mL KMnO4溶液。
回答下列问题。
写出H2C2O4和酸性KMnO4溶液反应的化学方程式_______;经计算x=_______。
(8)依据以上实验,写出草酸晶体(H2C2O4·xH2O)受热分解的化学方程式_______。
【答案】 冷凝草酸气体,防止草酸进入装置C反应生成沉淀而干扰CO2的检验。 Ca2++2OH-+CO2=CaCO3↓+H2O 吸收CO2气体,防止干扰CO气体的检验 碱石灰(或无水CaCl2) G中黑色粉末变为红色,其后的H中澄清石灰水变浑浊 Ⅰ 2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O 2 H2C2O4·2H2O![]() CO↑+ CO2↑+3H2O
CO↑+ CO2↑+3H2O
【解析】(1)草酸晶体受热易脱水、升华,装置B可以冷凝草酸气体,草酸钙难溶于水,同时装置B可以防止草酸进入装置C反应生成沉淀而干扰CO2的检验,故答案为:冷凝草酸气体,防止草酸进入装置C反应生成沉淀而干扰CO2的检验;
(2)装置C是检验生成的二氧化碳,反应的离子方程式为Ca2++2OH-+CO2=CaCO3↓+H2O,故答案为:Ca2++2OH-+CO2=CaCO3↓+H2O;
(3)装置D中的氢氧化钠可以除去剩余的二氧化碳气体,防止干扰CO气体的检验,故答案为:吸收CO2气体,防止干扰CO气体的检验;
(4)气体从溶液中经过会带有水蒸气,装置F是干燥生成的一氧化碳气体,可以选用的药品是碱石灰(或无水CaCl2)等固体干燥剂,故答案为:碱石灰(或无水CaCl2);
(5)若草酸晶体分解产物中有CO,则G中氧化铜会被还原为铜,看到的现象有G中黑色粉末变为红色,其后的H中澄清石灰水变浑浊,故答案为:G中黑色粉末变为红色,其后的H中澄清石灰水变浑浊;
(6)G出来的气体中还原二氧化碳和一氧化碳,可以用排水集气装置Ⅰ,除去二氧化碳并收集一氧化碳,故答案为:Ⅰ;
(7)H2C2O4和酸性KMnO4溶液反应生成二氧化碳和硫酸锰,反应的化学方程式为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O ; 12.50 mL 0.4 mol/L KMnO4溶液中还原高锰酸钾的物质的量为0.0125L×0.4 mol/L=0.005mol,由2MnO2-+5H2C2O4 +6H+═2Mn2++10CO2↑+8H2O可知,草酸的物质的量= 0.005mol×![]() =0.0125mol,6.3 g草酸晶体的物质的量=0.0125mol×
=0.0125mol,6.3 g草酸晶体的物质的量=0.0125mol×![]() =0.05mol=
=0.05mol= ![]() ,解得:x=2,故答案为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O ;2;
,解得:x=2,故答案为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O ;2;
(8)根据以上实验,草酸晶体(H2C2O4·xH2O)受热分解生成一氧化碳和二氧化碳,反应的化学方程式为H2C2O4·2H2O![]() CO↑+ CO2↑+3H2O,故答案为:H2C2O4·2H2O
CO↑+ CO2↑+3H2O,故答案为:H2C2O4·2H2O![]() CO↑+ CO2↑+3H2O。
CO↑+ CO2↑+3H2O。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案