题目内容
【题目】下列各表述与示意图一致的是
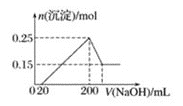
A. 如图表示向含
如图表示向含![]() 、
、![]() 、
、![]() 的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积关系图.则三种离子的物质的量之比为:
的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积关系图.则三种离子的物质的量之比为:![]() :
:![]() :
:![]()
![]() :1:2,其中使用的NaOH的浓度为2
:1:2,其中使用的NaOH的浓度为2![]()
B. 如图中曲线表示某反应过程的能量变化,当物质
如图中曲线表示某反应过程的能量变化,当物质![]() 与
与![]() 反应生成物质
反应生成物质![]() 是,
是,![]() ,若使用正催化剂,E值会减小
,若使用正催化剂,E值会减小
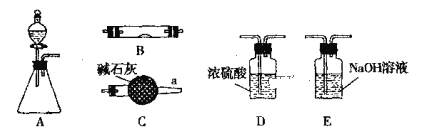
C.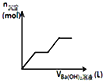 如图可用来表示向盐酸酸化的
如图可用来表示向盐酸酸化的![]() 溶液中加入
溶液中加入![]() 溶液时,产生沉淀的物质的量
溶液时,产生沉淀的物质的量![]() 与加入
与加入![]() 溶液体积
溶液体积![]() 之间的关系图
之间的关系图
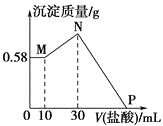
D. 如图表示向一定质量的明矾溶液中滴加
如图表示向一定质量的明矾溶液中滴加![]() 溶液时,产生沉淀的质量
溶液时,产生沉淀的质量![]() 与加入
与加入![]() 溶液体积
溶液体积![]() 之间的关系图
之间的关系图
【答案】C
【解析】
A.根据图①中各段含义,得到NaOH溶液为25mL到35mL是与NH4+反应,35mL到40mL是与氢氧化铝反应,剩余的为氢氧化镁,故得到n(Mg2+)=0.05mol,根据Al3+与NaOH反应沉淀与溶解时量的关系为3:1确定,与Mg2+反应的NaOH溶液体积为255×3=10mL,c(NaOH)=0.05×2÷0.01=10mol/L,根据35mL到40mL段得n(Al3+)=n(NaOH)=0.005×10=0.05mol,根据25mL到35mL段得n(NH4+)=n(NaOH)=0.01×10=0.1mol,n(Mg2+):n(Al3+):n(NH4+)=0.05mol:0.05mol:0.1mol=1:1:2,故A错误;
B.根据图②知反应物的总能量比生成物的总能量高,是放热反应,△H<0,使用催化剂改变反应的活化能,但不能改变反应的焓变,故B错误;
C.向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液后,先产生的沉淀只是BaSO4,然后是中和反应,最后是与Mg2+产生沉淀Mg(OH)2,故C正确;
D.向一定质量的明矾溶液中滴加Ba(OH)2溶液时,先发生的反应是2KAl(SO4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4,然后2Al(OH)3+K2SO4+Ba(OH)2=2KAlO2+BaSO4↓+H2O,即沉淀达最多后溶解一部分,故D错误;
答案选C。

 阅读快车系列答案
阅读快车系列答案