��Ŀ����
����Ŀ����ͼ��ʾΪ���������Ʊ������������֤��β�������IJ�������װ�ã������豸���г̶ֹ�װ�þ���ȥ���������Ҫ��������и��⣬����װ�ÿ�����ѡ�ã���Ҫʱ���ظ�ѡ��
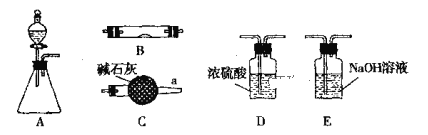
��1������ƿ��ʢװпƬ����Һ©����ʢװϡ���ᣬ����֤H2�Ļ�ԭ�Բ��������������
�ٵ���������˳��ΪA��D��B��B��Cʱ������ʹ��Bװ�ã�������ʢ��ҩƷ������CuO��____________��
�ڼ���װ�õ������Ժ����Bǰ������еIJ�����_________________ ��
��2������ƿ��ʢװNa2O2���壬��Һ©����ʢװŨ��ˮ��B��ʢװ����������ɽ��а��Ĵ��������䷴Ӧ����ΪNO��H2O��
�ٸ�����װ�ð������������������˳��A��C��B��C����д��B�а��Ĵ�������Ӧ����ʽ____________________________ ��
��װ��B�п��ܹ۲쵽��������_____________________________��
��3������ƿ��ʢװNa2SO3���壬��Һ©����ʢװH2SO4��Һ��B��ʢװNa2O2���壬��̽��SO2������������Ʒ�Ӧʱ�Ƿ���O2���ɡ�������������װ�õ�����˳��Ϊ��A��D��B��E������ʵ������ش����⣺
�������������ľ������E�ĵ��ܿڣ�ľ����ȼ��SO2������������������ʣ���Ӧ�ķ���ʽ����Ϊ��____________________��
������E�ĵ��ܿ�δ�ռ����κ����壬SO2ֻ���ֻ�ԭ�ԣ���Ӧ�ķ���ʽ����Ϊ��____________________��
��װ��B�й۲쵽��������__________��
���𰸡���ˮ����ͭ ���������Ƿ������װ���п����Ƿ��ž� 4NH3+5O2 ![]() 4NO+6H2O �к���ɫ������֣��������ڱڸ�����ˮ�� 2SO2+2Na2O2=2Na2SO3+O2 SO2+Na2O2=Na2SO4 ����ɫ�����ĩ��Ϊ��ɫ
4NO+6H2O �к���ɫ������֣��������ڱڸ�����ˮ�� 2SO2+2Na2O2=2Na2SO3+O2 SO2+Na2O2=Na2SO4 ����ɫ�����ĩ��Ϊ��ɫ
��������
��1������֤H2�Ļ�ԭ�ԣ����Ƚ���������ˮ��������ˮ����ͭ����ˮ���ڶ���ʹ��Bװ�õ������Ǽ������ˮ��
��������������ʱ��������������ը����˼���Bװ��ǰ��Ҫ���������Ĵ��ȣ�
��2���ٰ��Ĵ���������ΪNO��H2O��
�ڰ�����B�з�����������Ӧ����NO��NO�ֻ������O2��Ӧ����NO2����B�л���ֺ���ɫ���壬ͬʱ�����ڱڻ�����ˮ����֣�
��3���������������ľ������E�ĵ��ܿڣ�ľ����ȼ��˵��������������SO2������������������ʣ�����Ԫ�ػ��ϼ۲��䣬��Ӧ���������������ƺ�������
������E�ĵ��ܿ�δ�ռ����κ����壬SO2ֻ���ֻ�ԭ�ԣ���������Ʊ��������ԣ���Ӧ��������Na2SO4��
��װ��B��Na2O2��SO2��Ӧ����Na2SO3��Na2SO4�����߾�Ϊ��ɫ�����ĩ���ݴ˽��
��1������֤H2�Ļ�ԭ�ԣ����Ƚ���������ˮ��������ˮ����ͭ����ˮ��
�ʴ�Ϊ����ˮ����ͭ��
����H2���п�ȼ�ԣ����ڼ���CuOǰ�����ž�װ���ڵĿ��������жϿ����Ƿ��ž��ķ����Ǽ����װ���ڳ����������Ƿ���
�ʴ�Ϊ�����������Ƿ������װ���п����Ƿ��ž���
��2���ٰ��Ĵ������ķ�Ӧ����ʽΪ4NH3+5O2![]() 4NO+6H2O��
4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2![]() 4NO+6H2O��
4NO+6H2O��
�ڰ�����B�з�����������Ӧ����NO��NO�ֻ������O2��Ӧ����NO2����B�л���ֺ���ɫ���壬ͬʱ�����ڱڻ�����ˮ����֣�
�ʴ�Ϊ���к���ɫ������֣��������ڱڸ�����ˮ�飻
��3���������������ľ������E�ĵ��ܿڣ�ľ����ȼ��˵��������������SO2������������������ʣ�����Ԫ�ػ��ϼ۲��䣬��Ӧ�ķ���ʽ����Ϊ��2SO2+2Na2O2=2Na2SO3+O2��
�ʴ�Ϊ��2SO2+2Na2O2=2Na2SO3+O2��
������E�ĵ��ܿ�δ�ռ����κ����壬SO2ֻ���ֻ�ԭ�ԣ���������Ʊ��������ԣ���Ӧ�ķ���ʽ����Ϊ��SO2+Na2O2=Na2SO4��
�ʴ�Ϊ��SO2+Na2O2=Na2SO4��
��װ��B��Na2O2��SO2��Ӧ����Na2SO3��Na2SO4�����߾�Ϊ��ɫ�����ĩ����۲쵽�������ǵ���ɫ�����ĩ��Ϊ��ɫ��
�ʴ�Ϊ������ɫ�����ĩ��Ϊ��ɫ��

����Ŀ��2009��10��1�գ��ҹ��ɹ��ٰ������ʮ���ı���������ı���ʽ��9���綯�����϶�����������Դ���������࣬չʾ���ۺϹ����������Ƽ���չˮƽ��ͬʱҲ˵����Դ��ȱ������������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���
��Ӧ�� CO(g) �� 2H2(g)![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��Ӧ�� CO2(g) �� 3H2(g)![]() CH3OH(g) + H2O(g) ��H2
CH3OH(g) + H2O(g) ��H2
��������Ӧ������ԭ�Ӿ�����ԭ����� _____����������������������
���±����������Ƿ�Ӧ���ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
�¶� | 250�� | 300�� | 350�� |
K | 2.041 | 0.270 | 0.012 |
�ɱ��������ж���H1 0 ������������������������������
��ij�¶��£���2 mol CO��6 mol H2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c(CO)�� 0.2 mol/L����CO��ת����Ϊ ����ʱ���¶�Ϊ �����ϱ���ѡ��
��2����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) �� 3O2(g) �� 2CO2(g) �� 4H2O(g) ��H1����1275.6 kJ/mol
�� 2CO (g)+ O2(g) �� 2CO2(g) ��H2����566.0 kJ/mol
�� H2O(g) �� H2O(l) ��H3����44.0 kJ/mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ����
�������ͼ��ʾ�ĵ��װ�á��õ�������ĵ缫��ӦΪ ��

�ڹ���һ��ʱ������Һ��pH��С���õ���ܷ�Ӧ�Ļ�ѧ����ʽΪ
��