��Ŀ����
����Ŀ��I�������ֶ�����Ԫ�أ����ǵĽṹ�����ʵ���Ϣ���±�������
Ԫ�� | �ṹ�����ʵ���Ϣ |
A | �Ƕ������У���ϡ�������⣩ԭ�Ӱ뾶����Ԫ�أ���Ԫ�ص�ij�ֺϽ���ԭ�ӷ�Ӧ�ѵĵ��ȼ� |
B | B��Aͬ���ڣ�������������ˮ��������� |
C | Ԫ�ص���̬�⻯�K������ˮ������������� |
D | �Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ������ˮ���������г��õ�����ɱ���� |
����ݱ�����Ϣ��д��
��1��D���Ľṹʾ��ͼ��___��
��2��CԪ�ص���̬�⻯��Ļ�ѧʽΪ��___������鷽����___��
��3��BԪ�������ڱ��е�λ��___�����Ӱ뾶��B___A������ڡ���С�ڡ�����
��4��B������������Ӧ��ˮ������A������������Ӧ��ˮ���ﷴӦ�Ļ�ѧ����ʽΪ___����D���⻯���ˮ���ﷴӦ�����ӷ���ʽΪ___��
II����2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g��2NO2��g����ϵ�У�n��NO����ʱ��ı仯���±���
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

��1��NO��ƽ��Ũ��c/span>��NO����___��
��2��ͼ�б�ʾNO2�仯��������___����O2��ʾ0��2s�ڸ÷�Ӧ��ƽ����������___��
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����___��
a������NO2����2����O2�� b������������ѹǿ���ֲ���
c�����棨NO����2������O2�� d��������������ܶȱ��ֲ���
���𰸡� NH3 ����һ����ʪ��ĺ�ɫʯ����ֽ���飬��ֽ����֤���а��������������ò�����պŨ�������Ũ��������������̣�֤���а��� �������ڵڢ�A�� С�� Al��OH��3+NaOH�TNaAlO2+2H2O 3H++Al��OH��3�TAl3++3H2O 0.0035mol/L b 0.0015mol/��Ls�� bc
NH3 ����һ����ʪ��ĺ�ɫʯ����ֽ���飬��ֽ����֤���а��������������ò�����պŨ�������Ũ��������������̣�֤���а��� �������ڵڢ�A�� С�� Al��OH��3+NaOH�TNaAlO2+2H2O 3H++Al��OH��3�TAl3++3H2O 0.0035mol/L b 0.0015mol/��Ls�� bc
��������
I��A�Ƕ�������(��ϡ��������)ԭ�Ӱ뾶����Ԫ�أ���Ԫ�ص�ij�ֺϽ���ԭ�ӷ�Ӧ�ѵĵ��ȼ�������AΪ��Ԫ�أ�B��Aͬ���ڣ�������������ˮ��������ԣ���BΪ��Ԫ�أ�CԪ�ص���̬�⻯�K������ˮ�����������������CΪ��Ԫ�أ�D�Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ������ˮ���������г��õ�����ɱ��������DΪ��Ԫ�أ��ݴ˴��⡣
I���ɷ���֪��AΪNaԪ�ء�BΪAlԪ�ء�CΪNԪ�ء�DΪClԪ�أ�
(1)DΪClԪ�أ���Cl���Ľṹʾ��ͼ��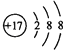 ��
��
(2)CΪNԪ�أ�����̬�⻯��Ļ�ѧʽΪNH3��������ˮ��Һ�Լ��ԣ����ü���NH3�ķ���������һ����ʪ��ĺ�ɫʯ����ֽ���飬��ֽ����֤���а��������������ò�����պŨ�������Ũ��������������̣�֤���а�����
(3)BΪAlԪ�أ��������ڱ��е�λ���ǵ������ڵڢ�A�壻Na+��Al3+������ͬ�ĵ��Ӳ�ṹ���˵���������Ӱ뾶С�������Ӱ뾶��Al3+С��Na+��
(4)Al(OH)3����NaOH����NaAlO2��ˮ��������Ӧ�Ļ�ѧ����ʽΪAl(OH)3+NaOH�TNaAlO2+2H2O��Al(OH)3����ϡ����ʱ������Ӧ�����ӷ���ʽΪ3H++Al(OH)3�TAl3++3H2O��
II.(1)3s��һ��������Ũ�ȱ��ֲ��䣬˵����Ӧ��ƽ��״̬������NO��ƽ��Ũ��c(NO)��![]() ��0.0035mol/L��
��0.0035mol/L��
(2)��(1)�����֪��ƽ��ʱ����������Ũ��Ϊ0.0065 mol/L���Ҷ�������Ϊ���������ʱ������ƶ�������Ũ����������bƽ��ʱ��Ũ��Ϊ0.0065mol/L��������b��ʾNO2��Ũ�ȱ仯����ͼ�����ݿ�֪2s�ڣ�NO��Ũ�ȱ仯��Ϊ0.01mol/L��0.004mol/L��0.006mol/L������(NO)��![]() ��0.003mol/(Ls)����������֮�ȵ��ڻ�ѧ������֮�ȣ�����(O2)��
��0.003mol/(Ls)����������֮�ȵ��ڻ�ѧ������֮�ȣ�����(O2)��![]() ��(NO)��
��(NO)��![]() ��0.003mol/(Ls)��0.0015mol/(Ls)��
��0.003mol/(Ls)��0.0015mol/(Ls)��
(3)a.δָ���������ʣ�����Ϊͬһ�������ʣ�ʼ�ն�������(NO2)��2��(O2)��ϵ���ʲ���˵������ƽ�⣬��Ϊ��ͬ��������ʣ�����֮�ȵ��ڻ�ѧ������֮�ȣ�˵������ƽ�⣬��
b.�淴Ӧ������������ʵ�����С��ѹǿ��С��������ѹǿ���ֲ��䣬˵������ƽ�⣻
c.��ͬ���ʱ�ʾ����������֮�ȵ��ڻ�ѧ������֮�ȣ���Ӧ����ƽ�⣬������(NO)��2����(O2)˵������ƽ�⣻
d.��Ӧ���������������䣬������������䣬�ܶ�ʼ�ղ��䣬�����������ʵ��ܶȱ��ֲ��䣬����˵������ƽ�⣻
�ʴ�Ϊbc��

����Ŀ���ݹ�����2019��12��ͳ�ƣ�2019��ȫ���������������Ѵ�3.5�ڡ�����β���ŷŵ�̼�⻯����������Pһ����̼��������д�����Ⱦ����Ҫ��Ⱦ����Ļ�����ϳɡ�Ӧ�ü����Ĺ̶�һֱ�ǿ�ѧ�о����ȵ㡣
I: (1)��CO2��NH3Ϊԭ�Ϻϳɻ������ص���Ҫ��Ӧ���£�
��2NH3(g)��CO2(g)��NH2CO2NH4(s)����H1����159.47 kJ��mol1
��NH2CO2NH4(s)��CO(NH2)2(s)��H2O(g)����H2��a kJ��mol1
��2NH3(g)��CO2(g)��CO(NH2)2(s)��H2O(g)����H3����86.98 kJ��mol1
��aΪ______��
(2)���ؿ�����ʪ�������ѵ����գ��䷴Ӧԭ��Ϊ��NO��NO2��H2O��2HNO2��2HNO2��CO(NH2)2��2N2����CO2����3H2O��
�ٵ�������NO��NO2��������Ӧ��ϵ����ʱ�ѵ�Ч����ѡ���������V(NO)��V(NO2)��5��1ʱ����ͨ��һ�����Ŀ�����ͬ��ͬѹ�£�V(����)��V(NO)��______(���������������������ԼΪ20%)��
����ͼ1��ʾ���غ������ѵ�Ч�ʵ�Ӱ�죬�Ӿ��������Ͽ��ǣ�һ��ѡ������Ũ��ԼΪ______%��

(3)ͼ2��ʾʹ�����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl-NH4ClΪ�������Һ����������ṩ������ͬʱ����ʵ�ֵ��̶�������ȼ�ϵ�ء���д���õ�ص�������Ӧʽ______�������пɷ����������A�Ļ�ѧʽΪ______��
II: ���ݻ�Ϊ2L���ܱ������м������̿![]() ����
����![]() ��NO��������Ӧ:
��NO��������Ӧ:![]()
![]()
![]() ��H��0��NO��
��H��0��NO��![]() �����ʵ����仯���±���ʾ��
�����ʵ����仯���±���ʾ��
���ʵ��� |
| T2/0C | |||||
0 |
|
|
|
|
|
| |
NO |
|
|
|
|
|
|
|
| 0 |
|
|
|
|
|
|
(1)T1���¶��£���Ӧ������![]() ���ö�����̼��ʾ�÷�Ӧ��ƽ����Ӧ����
���ö�����̼��ʾ�÷�Ӧ��ƽ����Ӧ����![]() ______����֪�������ѹ
______����֪�������ѹ![]() ������ѹ
������ѹ![]() ���������
���������![]() ʱ��ƽ���ѹ����ƽ��Ũ�ȼ���ƽ�ⳣ��
ʱ��ƽ���ѹ����ƽ��Ũ�ȼ���ƽ�ⳣ��![]() ______��
______��
![]() ��
��![]() ���¶ȵ�����
���¶ȵ�����![]() �����ݱ仯���ϱ���ʾ����
�����ݱ仯���ϱ���ʾ����![]() ______
______![]() �
�![]() ����
����![]() ����
����![]() ��
��![]() ��
��
(3)��30minʱ������![]() ���䣬����������ټ�������ַ�Ӧ������
���䣬����������ټ�������ַ�Ӧ������![]() �����ʱ��Ӧ______�ƶ�
�����ʱ��Ӧ______�ƶ�![]() �����������
�����������![]() ��
��