��Ŀ����
19��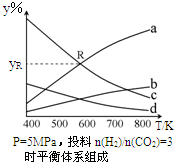 ��CO2Ϊ̼Դ��ȡ��̼�л����Ϊ�����о����㣬����ΪCO2������ȡ�Ҵ��ķ�Ӧ��2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��g����H=QkJ/mol ��Q��0�����ܱ������У���CO2��H2�����ʵ���֮��Ϊ1��3����Ͷ�ϣ���5MPa�²�ò�ͬ�¶���ƽ����ϵ�и������ʵ����������y%����ͼ��ʾ��
��CO2Ϊ̼Դ��ȡ��̼�л����Ϊ�����о����㣬����ΪCO2������ȡ�Ҵ��ķ�Ӧ��2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��g����H=QkJ/mol ��Q��0�����ܱ������У���CO2��H2�����ʵ���֮��Ϊ1��3����Ͷ�ϣ���5MPa�²�ò�ͬ�¶���ƽ����ϵ�и������ʵ����������y%����ͼ��ʾ�����������գ�
��1����ʾCH3CH2OH����������ߵ���b��ѡ����ţ���
��2����һ���¶��·�Ӧ�ﵽƽ��ı�־��BC��
A��ƽ�ⳣ��K��������
B��CO2��ת���ʲ�������
C����������ƽ����Է����������ٸı�
D����Ӧ�ﲻ��ת��Ϊ������
��3�����������㶨���ﵽƽ��������H2ת���ʵĴ�ʩ��AC��ѡ���ţ��� A�������¶� B����������H2 C����ȥ�Ҵ� D�������������
��4��ͼ������a��c�Ľ���R��Ӧ���ʵ��������yR=37.5%��
���� ��1���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ��ʱCO2��H2�ĺ������ͣ�CH3CH2OH��H2O�ĺ�������ʼCO2 ��H2 �����ʵ���֮��1��3���У�ƽ��ʱH2�ĺ�����CO2�ĺ���������CH3CH2OH��H2O��1��3���ɣ�ƽ��ʱH2O�ĺ�����CH3CH2OH������������
��2����ѧ��Ӧ�ﵽ��ѧƽ��״̬ʱ�����淴Ӧ������ȣ��Ҳ�����0�������ʵ�Ũ�Ȳ��ٷ����仯���ɴ�������һЩ�������������仯���Դ˽����жϣ��ó���ȷ���ۣ�
��3��������������Է�Ӧ���ʵ�Ӱ������жϣ�
��4��R��Ϊa��c�Ľ��㣬���ʱa��H2O���ΪV����ôc��H2���ҲΪV�����ݷ���ʽ�еĹ�ϵ���CO2��CH3CH2OH������������������ya��
��� �⣺��1���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ��ʱCO2��H2�ĺ������ͣ�CH3CH2OH��H2O�ĺ�������ʼCO2 ��H2 �����ʵ���֮��1��3���У�ƽ��ʱH2�ĺ�����CO2�ĺ���������CH3CH2OH��H2O��1��3���ɣ�ƽ��ʱH2O�ĺ�����CH3CH2OH������������
����a������b���¶����ߺ�������������a�ĺ����ߣ���������a��ʾH2O������b��ʾCH3CH2OH��
����c������d���¶����ߺ�����С��������c�ĺ����ߣ���������c��ʾH2������d��ʾCO2��
�ʴ�Ϊ��b��
��2��A��ƽ�ⳣ��Kֻ���¶��йأ����Ƿ�ﵽƽ��״̬�أ���A����
B��CO2��ת���ʲ�������˵���ﵽƽ��״̬����B��ȷ��
C��ƽ��������=$\frac{������}{�����ʵ���}$�����������䣬�����ʵ�����䣬�ʻ�������ƽ����Է����������ٸı����Ϊ�ж��Ƿ�ﵽ��ѧƽ��״̬�����ݣ���C��ȷ��
D���÷�Ӧ�ǿ��淴Ӧ�������ڷ�Ӧ�ﲻ��ת��Ϊ�������״̬����D����
�ʴ�Ϊ��BC��
��3��A�������¶ȣ�ƽ�������ƶ���������ת��������
B����������H2��ƽ�������ƶ���������ת���ʽ��ͣ�
C����ȥ�Ҵ���ƽ�������ƶ���������ת��������
D���������������ѹǿ��С��ƽ�������ƶ���������ת���ʽ��ͣ�
�ʴ�Ϊ��AC��
��4��2CO2��g��+6H2��g��=CH3CH2OH��g��+3H2O��g����
R��Ϊa��c�Ľ��㣬���ʱa��H2O���Ϊ6V����ôc��H2���ҲΪ6V�����ݷ���ʽ��֪CO2Ϊ$\frac{6V}{6}$=2V��C2H5OHΪ$\frac{6V}{3}$=2V��
����R���Ӧ���������ya=$\frac{6V}{6V+6V+2V+2V}$��100%=37.5%��
�ʴ�Ϊ��37.5%��
���� ���⿼��ѧ����ͼ��ķ�����ƽ���ƶ���ƽ��״̬�����������⣬�ѶȽϴ�ע���ж����߱�ʾ��һ���ʵ���������ǹؼ���

| A�� | ʵ������п��ϡ���ᷴӦʱ���μ���������ͭ��Һ�ܼӿ췴Ӧ���ʣ���Ϊ����ͭ�Ǵ��� | |
| B�� | ij�¶��£�һ��������ܱ������н��п��淴Ӧ��X��g��+Y��g��=Z��g��+W��g����H��0��ƽ������һ����X�����H���� | |
| C�� | �¶Ⱥ�ѹǿһ��ʱ�����ڿ��淴Ӧ��2NO2��g��?N2O4��g�������������ܶȲ��ٸı䣬��Ӧ�ﵽƽ��״̬ | |
| D�� | ��NaAlO2��Һ��NaHCO3��Һ��Ϻ����ɰ�ɫ��������������Һˮ����ٽ��Ľ�� |
| A�� | NH4+��Ag+��NO3-��CO32-��SO42- | B�� | Fe2+��H+��NO3-��Cl- | ||
| C�� | Al3+��NH4+��HCO3-��Cl- | D�� | K+��Na+��NO3-��SO42- |
| A�� | ��X��Y����ͬһ���ڣ���X��ԭ�Ӱ뾶�϶�С��Y��ԭ�Ӱ뾶 | |
| B�� | ��M�������ӻ������û�������ֻ�������Ӽ�����ÿ��ԭ�Ӿ��ﵽ8�����ȶ��ṹ | |
| C�� | ������������X��Y��2����X�ķǽ�����һ����Y�ķǽ�����ǿ | |
| D�� | ��X��Y����ͬһ���ڣ���M���ڹ��ۻ�����������ԭ�Ӹ����ȿ���Ϊ1��2 |
| A�� | X��Y����ȼ�գ����д���Ũ�̲��� | |
| B�� | X����ʹ���Ը��������Һ��ɫ��Ҳ��ʹ��ˮ��ɫ�����ܷ����Ӿ۷�Ӧ | |
| C�� | Y���ڲ������� | |
| D�� | Y�Ķ��ȴ��������� |
| X | ||
| M | Y | Z |
| A�� | ԭ�Ӱ뾶��СΪZ��Y��M��X | |
| B�� | ����������ˮ���������ǿ��ΪX��Z��Y��M | |
| C�� | ���γɼ����ӣ������Ӱ뾶��СΪM��Y��Z��X | |
| D�� | X��M��Y��M������ͬΪ����Ԫ�� |
 ����ѡ���еķ�Ӧ�������������ȫһ�µ��ǣ��г֡�����װ������ȥ����������
����ѡ���еķ�Ӧ�������������ȫһ�µ��ǣ��г֡�����װ������ȥ����������| ���еķ�Ӧ | ���е����� | ���� | |
| A | MnO2��Ũ������� | KI������Һ�ܿ���� | Cl2�������� |
| B | Cu��Ũ������� | ��ˮ��ɫ | SO2��Ư���� |
| C | Na2CO3�������Һ | ��������Һ����� | ���ԣ�̼����� |
| D | ��ʯ�뱥��ʳ��ˮ | ���Ը��������Һ��ɫ | ��Ȳ�л�ԭ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ��0.01mol/L�Ĵ����pHΪ5��CH3COOH?CH3COO-+H+ | |
| B�� | ��ⱥ��ʳ��ˮ���������壺2Cl-+2H2O$\frac{\underline{\;����\;}}{\;}$Cl2��+2OH-+H2�� | |
| C�� | ������������ȼ�գ�������ɫ���壺4Fe+3O 2$\frac{\underline{\;��ȼ\;}}{\;}$2Fe2O3 | |
| D�� | �������̼������Һ��������ɫ������CaSO4��S��+CO32-?CaCO3��S��+SO42- |
| A�� | Ԫ��X������ͬλ�� | |
| B�� | ����һ��ͬλ��������Ϊ36 | |
| C�� | ������Ϊ35��ͬλ��ԭ�ӵ���������Ϊ75% | |
| D�� | Ԫ�ص���X2��ƽ��ʽ��Ϊ71 |