题目内容
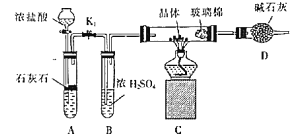
【题目】已知:硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全。确定分解产物的成分。

(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和___。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中定有___气体产生,写出D中发生反应的离子方程式__。若去掉C,是否能得出同样结论并解释其原因___。
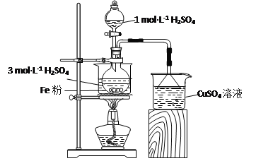
(3)为验证A中残留物是否含有FeO,需要选用的试剂有___。
A.KSCN溶液 B.稀硫酸 C.浓盐酸 D.KMnO4溶液
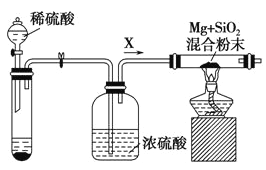
(4)已知分解产物中的某气体能使紫色石蕊试液变蓝,该气体被氧气连续氧化为红棕色气体,第一步催化氧化的化学反应方程式为:__。
(5)上述红棕色气体易溶于水,当该气体与氧气按5:1的体积比混合后装满试管倒置于水中,待液面稳定后试管中的气体体积变为原体积的__。
(6)E中收集到的气体只有N2,其物质的量为xmol,固体残留物Fe2O3的物质的量为ymol,D中沉淀物质的量为zmol,根据氧化还原反应的基本规律,x、y和z应满足的关系为__。
【答案】SO2 SO2 H2O2+SO2+Ba2+=2H++BaSO4↓ 不能,若有SO3也有白色沉淀产生 BD 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O ![]() 3x+y=z
3x+y=z
【解析】
(1)该反应为氧化还原反应,根据化合价升降守恒规律进行判断;
(2)C中无明显现象,D中有白色沉淀生成说明SO2被H2O2氧化后生成SO3,与氯化钡反应生成硫酸钡沉淀; SO3若存在也会出现同样的现象;
(3)验证A中残留物是否含有FeO,可将残留物溶于硫酸中,加入KMnO4溶液,观察KMnO4溶液是否褪色;
(4)能使紫色石蕊试液变蓝的气体是NH3,NH3催化氧化后能生成NO和水;
(5)红棕色气体为NO2,与水反应生成HNO3和NO;
(6)根据化合价升降守恒判断。
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,铁和氮的化合价升高,只能硫的化合价降低,所以气体产物可能有NH3、SO3、H2O、N2和SO2;
(2)实验中,观察到C中无明显现象,说明没有SO3生成,D中有白色沉淀生成,可确定产物中定有SO2气体产生,则D中发生反应的离子方程式H2O2+SO2+Ba2+=2H++BaSO4↓;若有SO3也有白色沉淀产生;若去掉C,不能得出同样结论;
(3)为验证A中残留物是否含有FeO,可将残留物溶于硫酸中,加入KMnO4溶液,观察KMnO4溶液是否褪色,因此需要选用的试剂有稀硫酸和KMnO4溶液;
(4)已知分解产物中的某气体能使紫色石蕊试液变蓝,该气体被氧气连续氧化为红棕色气体,则该气体为NH3,第一步催化氧化的化学反应方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(5)上述红棕色气体NO2和氧气混合溶于水,反应方程式为4NO2+O2+2H2O=4HNO3,当该气体与氧气按5:1的体积比混合后装满试管倒置于水中,剩余气体为1体积NO2,3NO2+H2O=2HNO3+NO,所以待液面稳定后试管中的气体体积变为原体积的![]() ×
×![]() =
=![]() ;
;
(6)E中收集到的气体只有N2,其物质的量为xmol,固体残留物Fe2O3的物质的量为ymol,D中沉淀BaSO4物质的量为zmol,根据氧化还原反应的基本规律,化合价升降总数相等,则x、y和z应满足的关系为6x+2y=2z,即3x+y=z。

 阅读快车系列答案
阅读快车系列答案