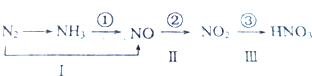题目内容
19.提纯液体有机物常采用的操作方法有蒸馏(分馏)、萃取分液.分析 提纯液体有机物可利用沸点差异或溶解性差异分离,以此来解答.
解答 解:若液体混合物互溶,但沸点不同,可采取蒸馏(分馏)法分离提纯,
若液体在不同溶剂的溶解性不同,选择萃取剂萃取分液分离提纯,
故答案为:蒸馏(分馏);萃取分液.
点评 本题考查物质分离提纯方法的选择和应用,为高频考点,把握物质的性质、性质差异及混合物分离原理为解答的关键,题目难度不大.

练习册系列答案
相关题目
7.相同条件下,用下列物质做氧化剂收集相同Cl2消耗浓盐酸最多的是( )
| A. | MnO2 | B. | KMnO4 | C. | NaClO | D. | KClO3 |
14.用沉淀法测定NaHCO3和K2CO3混合物的组成.实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液,每次实验均充分反应.实验记录见下表:
回答下列问题:
(1)写出少量NaHCO3和过量Ba(OH)2溶液反应的离子方程式Ba2++HCO3-+OH-═BaCO3↓+H2O.
(2)第2次实验中产生沉淀的质量是2.758g.
(3)样品中NaHCO3和K2CO3的物质的量之比是2:5.
(4)原Ba(OH)2溶液的浓度为0.056mol•L-1.
(5)室温下取第3组实验所得溶液的1/10,加水配成500mL溶液,则稀释以后溶液的pH值为12.
| 实验次数 | 称取样品的质量/g | 所加Ba(OH)2溶液的体积/mL | 测得生成沉淀的质量/g |
| 1 | 0.858 | 500 | 1.379 |
| 2 | 1.716 | 500 | |
| 3 | 2.574 | 500 | 4.137 |
| 4 | 3.432 | 500 | 5.516 |
| 5 | 4.290 | 500 | 5.516 |
| 6 | 5.148 | 500 | 5.516 |
(1)写出少量NaHCO3和过量Ba(OH)2溶液反应的离子方程式Ba2++HCO3-+OH-═BaCO3↓+H2O.
(2)第2次实验中产生沉淀的质量是2.758g.
(3)样品中NaHCO3和K2CO3的物质的量之比是2:5.
(4)原Ba(OH)2溶液的浓度为0.056mol•L-1.
(5)室温下取第3组实验所得溶液的1/10,加水配成500mL溶液,则稀释以后溶液的pH值为12.
4.BaSO4饱和溶液中加少量的BaCl2溶液产生BaSO4沉淀,若以Ksp表示BaSO4的溶度积常数,则平衡后溶液中( )
| A. | c (Ba2+)=c(SO42-)=(Ksp)${\;}^{\frac{1}{2}}$ | B. | c(Ba2+)•c(SO42-)>Ksp,c(Ba2+)=c(SO42-) | ||
| C. | c(Ba2+)•c(SO42-)=Ksp,c(Ba2+)>c(SO42-) | D. | c(Ba2+)•c(SO42-)≠Ksp,c(Ba2+)<c(SO42-) |
8.某种合金的晶胞结构如图所示,则下列说法正确的是( )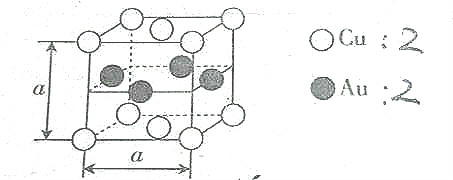

| A. | 该合金属于离子晶体 | B. | 该合金中Au的配位数是4 | ||
| C. | 该合金中Cu的配位数是8, | D. | 该合金的硬度低于Cu |
13.ClCH=CH-CH3能发生的反应有( )
①加聚 ②与硝酸银溶液生成白色沉淀 ③使溴水褪色 ④消去 ⑤加成 ⑥取代.
①加聚 ②与硝酸银溶液生成白色沉淀 ③使溴水褪色 ④消去 ⑤加成 ⑥取代.
| A. | 都可以 | B. | 只有①不能发生 | C. | 只有②不能发生 | D. | 只有①④不能发生 |
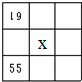

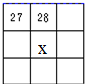
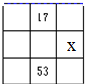
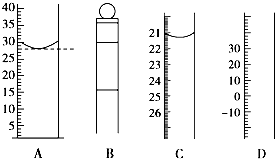 (1)图为常见仪器的部分结构(有的仪器被放大)
(1)图为常见仪器的部分结构(有的仪器被放大)