题目内容
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(铜元素、硫元素的存在形式分别为Cu2+、SO42-)加入足量NaOH稀溶液,产生蓝色沉淀,过滤,洗涤,灼烧沉淀,得到CuO固体12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则VL可能为
| A.7.5L | B.9.5L | C.13.6L | D.16.8L |
B
解析试题分析:若混合物全是CuS,其物质的量为10=0.15mol,电子转移数,0.15×(6+2)=1.2mol。两者体积相等,设NO xmol,NO2 xmol,3x+x1=1.2,计算的x=0.3。气体体积V=0.6×22.4=13.44L;若混合物全是Cu2S,其物质的量为0.075mol,转移电子数0.075×10=0.75mol, 设NO xmol,NO2 xmol, 3x+x1=0.75,计算得x=0.1875,气体体积0.375×22.4=8.4L,因此选B。
考点:考查了氧化还原反应的计算。

对剧毒的氰化物可在碱性条件下用如下方法进行处理:
2CN- +8OH-+5Cl2= 2CO2 +N2 +10Cl- +4H2O 下列判断正确的是
| A.当有0.2 mol CO2生成时,溶液中阴离子的物质的量增加1mol |
| B.该反应中,每有2molCN-反应,转移电子为10mol |
| C.上述反应中的还原剂是OH- |
| D.还原性:Cl-> CN- |
人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,主要由于维生素C具有
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
下列反应中必须加入还原剂才能进行的是
| A.Zn→Zn2+ | B.H2→H2O | C.CaO→Ca(OH)2 | D.CuO→Cu |
下列反应需要加入氧化剂才能实现的是
| A.Cl2→Cl- | B.H+ →H2 | C.MnO2 →Mn2+ | D.Zn→Zn2+ |
下列变化中,需要加入氧化剂才能实现的是( )
| A.HCl→H2 | B.FeO→Fe2+ | C.SO2→SO3 | D.CO32-→CO2 |
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-(其中碳元素为+2价)、HCO3-、N2、Cl-六种物质.在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是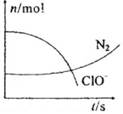
| A.还原剂是含CN-的物质,氧化产物只有N2 |
| B.氧化剂是ClO-,还原产物是HCO3- |
| C.配平后氧化剂与还原剂的化学计量数之比为5:2 |
| D.若生成2.24LN2(标准状况),则转移电子0.5mol |
已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2氧化性依次减弱。下列反应在水溶液中不可能发生的是
| A.Co2O3 + 6 HCl=2CoCl2 + Cl2↑+ 3H2O |
| B.Cl2 + FeI2 = FeCl2 + I2 |
| C.3 Cl2 + 6 FeI2 = 2FeCl3 + 4 FeI3 |
| D.2Fe3+ + 2I— = 2Fe2++ I2 |
含铬Cr2O72-废水用硫亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到nmolFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是
| A.消耗硫酸亚铁铵的物质量为n(3x+1)mol | B.处理废水中Cr2O72-的物质量为 mol mol |
| C.反应中发生转移的电子数为1.5nxmol | D.在FeO·FeyCrxO3中3x=y |