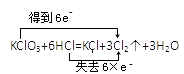
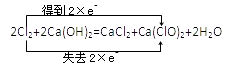��Ŀ����
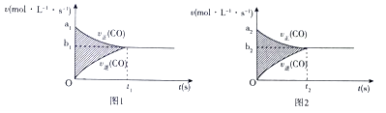
����Ŀ��ij���淴Ӧ��mA������+nB������pC���������ʱ�Ϊ��H�������¶�T��ʱ��t��������C������ٷ���C%��ƽ���������ƽ����Է�������M�Ĺ�ϵ��ͼ1��2��ʾ�����н�����ȷ���ǣ� �� 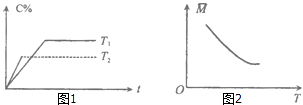
A.m+n��p����H��0
B.m+n��p����H��0
C.m+n��p����H��0
D.m+n��p����H��0
���𰸡�B
���������⣺���ݡ��ȹ���ƽ��ֵ��֪����ͼ��T2��T1 �� �����¶�C�ĺ�����С��˵��ƽ�����淴Ӧ�����ƶ���������Ӧ�Ƿ��ȷ�Ӧ�����ԡ�H��0��
������ͼ֪�������¶ȣ�ƽ�����淴Ӧ�����ƶ���ƽ����Է���������С����Ϊ��Ӧǰ���������䣬��˵���淴Ӧ����Ϊ�����������ķ���Ӧ����m+n��p��
��ѡB��
���ݡ��ȹ���ƽ��ֵ��֪����ͼ��T2��T1 �� �����¶�C�ĺ�����С��˵��ƽ�����淴Ӧ�����ƶ���������Ӧ�Ƿ��ȷ�Ӧ��
������ͼ֪�������¶ȣ�ƽ�����淴Ӧ�����ƶ���ƽ����Է���������С����Ϊ��Ӧǰ���������䣬��˵���淴Ӧ����Ϊ�����������ķ��ݴ˷������

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ