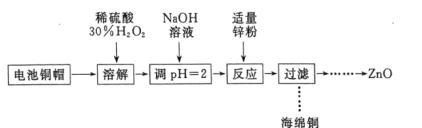
��Ŀ����
����Ŀ����ѧʵ����ͻ�����Ч�ؼ�����Ⱦ��ʵ�ֻ�ѧʵ����ɫ����Ҫ��ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1 mol/L��KBr��KI����������Һ����NaOH������̪����FeCl2����KSCN����Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ��(����ͼ��ʾ)����Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ�������ñ�����Ǻá�����֪2KMnO4+16HCl(Ũ)![]() 2KCl+2MnCl2+5Cl2��+8H2O��
2KCl+2MnCl2+5Cl2��+8H2O��

(1)e����Ӧ�����ӷ���ʽΪ_________________________________________���÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ_______________________��
(2) d����ʵ������__________________________________________��
(3)c����Ӧ�Ļ�ѧ����ʽΪ_________________________________����״���£�����0.224 L Cl2��NaOH��Һ���պ�ת�Ƶ��ӵ����ʵ���Ϊ__________mol��
(4)ͨ����ʵ���ܷ�Ƚ�Cl2��FeCl3��KMnO4�������������Ե�ǿ����__________�������������������� �������ܣ�����������ǿ������˳����____________________��
���𰸡�2MnO4-+16H++10Cl-=2Mn2++5Cl2��+8H2O 1:5 ��Һ��dz��ɫ��Ϊ��ɫ Cl2+2NaOH=NaCl+NaClO+H2O 0.01 �� KMnO4��Cl2��FeCl3
��������
���������Ļ�ѧ���ʼ�������ԭ��Ӧ�Ĺ��ɽ��з�����
(1)e��������غ�Ũ���ᷢ����Ӧ�����������÷�Ӧ�����ӷ���ʽΪ2MnO4-+16H++10Cl-=2Mn2++5Cl2��+8H2O���÷�Ӧ�и����������������Ũ����ȱ��ֻ�ԭ���ֱ������ԣ������ӷ���ʽ��֪���÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1:5��
(2) �Ȼ�������Һ��dz��ɫ��d���Ȼ���������������Ϊ�Ȼ�����+3�������������軯����Һ���Ժ�ɫ����ʵ������Ϊ��Һ��dz��ɫ��Ϊ��ɫ��
(3)c������������������Һ������Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪCl2+2NaOH=NaCl+NaClO+H2O����״���£� 0.224 L Cl2�����ʵ���Ϊ0.01mol���䱻NaOH��Һ���պ�ת�Ƶ��ӵ����ʵ���Ϊ0.01mol ��
(4)��ʵ���� KMnO4��Ũ��������ΪCl2��Cl2���Ȼ���������ΪFeCl3����ˣ�ͨ����ʵ���ܱȽ�Cl2��FeCl3��KMnO4���������������Ե�ǿ��������������ǿ������˳����KMnO4��Cl2��FeCl3��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�