题目内容
13. 硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:
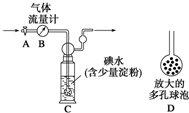
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积.将尾气通入一定体积已知浓度的碘水中测定SO2的含量.当洗气瓶C中溶液蓝色消失时,立即关闭活塞A.
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是增大SO2与碘水的接触面积,使SO2和碘水充分反应.
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量偏低 (填“偏高”、“偏低”或“无影响”).
乙方案:实验步骤如图所示:尾气VL$→_{①}^{过量H_{2}O_{2}溶液}$溶液$→_{②}^{过量Ba(OH)_{2}溶液}$ $→_{干燥、称重③}^{过滤、洗涤}$固体mg
(3)步骤③中洗涤沉淀的方法是向漏斗里注入蒸馏水,使水面没过沉淀物,待水流尽后,重复操作2~3次.
(4)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为$\frac{22.4m}{233V}$×100% (用含有V、m的代数式表示).如果将双氧水换成足量用稀硫酸酸化的高锰酸钾溶液,方案是否合理否,如不合理,如何改进将硫酸酸化的高锰酸钾溶液换成溴水或硝酸溶液(认为合理可不填).
分析 甲方案利用的原理为:SO2+I2+2H2O=H2SO4+2HI,据此确定二氧化硫的物质的量,进而定尾气中二氧化硫的含量,
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以增大SO2与碘水的接触面积,使SO2和碘水充分反应;
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,则通入尾气的体积增大;
乙方案利用的原理为:SO2+H2O2=H2SO4,H2SO4+Ba(OH)2=BaSO4↓+2H2O,最后沉淀硫酸钡的质量计算尾气中二氧化硫的质量,进而计算尾气二氧化硫含量;
(3)洗涤沉淀的方法是:向漏斗里注入蒸馏水,使水面没过沉淀物,待水流尽后,重复操作2~3次;
(4)mg是硫酸钡的质量,计算硫酸钡的物质的量,根据硫元素守恒计算二氧化硫的体积,进而计算二氧化硫的体积分数;如果将双氧水换成足量用稀硫酸酸化的高锰酸钾溶液,得到沉淀不是二氧化硫被氧化生成的硫酸生成的沉淀,酸化高锰酸钾溶液的硫酸也会生成硫酸钡沉淀.
解答 解:甲方案利用的原理为:SO2+I2+2H2O=H2SO4+2HI,最后测定剩余气体的体积,进而定尾气中二氧化硫的含量,
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以增大SO2与碘水的接触面积,使SO2和碘水充分反应,
故答案为:增大SO2与碘水的接触面积,使SO2和碘水充分反应;
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,则通入尾气的体积增大,因此SO2含量偏低,
故答案为:偏低;
乙方案利用的原理为:SO2+H2O2=H2SO4,H2SO4+Ba(OH)2=BaSO4↓+2H2O,最后沉淀硫酸钡的质量计算尾气中二氧化硫的质量,进而计算尾气二氧化硫含量,
(3)洗涤沉淀的方法是:向漏斗里注入蒸馏水,使水面没过沉淀物,待水流尽后,重复操作2~3次,
故答案为:向漏斗里注入蒸馏水,使水面没过沉淀物,待水流尽后,重复操作2~3次;
(4)mg是硫酸钡的质量,硫酸钡的物质的量为$\frac{mg}{233g/mol}$=$\frac{m}{233}$mol,根据硫元素守恒可知二氧化硫的体积为$\frac{m}{233}$mol×22.4L/mol=$\frac{22.4m}{233}$L,故尾气中二氧化硫的体积分数$\frac{22.4m}{233}$×100%=$\frac{22.4m}{233V}$×100%;如果将双氧水换成足量用稀硫酸酸化的高锰酸钾溶液,酸化高锰酸钾溶液的硫酸也会和钡离子生成硫酸钡沉淀,无法计算二氧化硫的量,方案不合理,应将硫酸酸化的高锰酸钾溶液换成溴水或硝酸溶液做氧化剂,
故答案为:$\frac{22.4m}{233V}$×100%,否,将硫酸酸化的高锰酸钾溶液换成溴水或硝酸溶液.
点评 本题考查学生对实验原理与实验操作的理解、实验方案设计、元素化合物性质、化学计算等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

 每课必练系列答案
每课必练系列答案| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 | |
| C. | 用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
| A. | 2.0 | B. | 2.3 | C. | 3.0 | D. | 7.0 |
| A. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O | |
| C. | Fe (NO3)2与HI的反应:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O | |
| D. | 少量SO2通入漂白粉溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO |
| A. | 相同条件下,在水中碳酸钠的溶解度小于碳酸氢钠的溶解度 | |
| B. | 氧化钠和过氧化钠都能与二氧化碳反应,生成物完全相同 | |
| C. | 碳酸氢钠固体中混有少量碳酸钠,可用加热的方法除去 | |
| D. | 质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,后者产生气体多 |
| A. | 只有②④⑤ | B. | 只有①③④ | C. | ①②③④⑤ | D. | 只有①②③④ |
 短周期元素X、Y、Z、W、E、Q在元素周期表中的位置如图所示,其中X、Y、Z三种元素的质子数之和为21.回答下列问题
短周期元素X、Y、Z、W、E、Q在元素周期表中的位置如图所示,其中X、Y、Z三种元素的质子数之和为21.回答下列问题| X | Y | Z | W |
| E | Q |
①Cl2O+H2O=2HClO②OF2+H2O═2HF+O2
(2)E元素的一种单质A,分子空间构型为正四面体,键角为60°,写出A(A被氧化成最高价含氧酸)与Y的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式3P4+20HNO3+8H2O=12H3PO4+20NO↑,工业上使用Ca3(EO4)2、石英砂和焦炭粉在电弧炉中熔烧还原得到A,化学方程式为:2Ca3(PO4)2+6SiO2+10C$\frac{\underline{\;电弧熔烧\;}}{\;}$P4+6CaSiO3+10CO↑.
(3)磷有多种化合物,次磷酸(H3PO2,为一元中强酸)和次磷酸钠(NaH2PO2)是化工生产中常用的还原剂.
①化学镀银,可利用H3PO2把溶液中的Ag+还原为银的反应,已知该反应中还原剂与氧化剂的物质的量之比为1:4,则氧化产物是H3PO4(填化学式).
②工业上可用白磷(P4)与Ba(OH)2溶液反应生成PH3和Ba(H2PO2)2.写出并配平该反应的化学方程式2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑,
如图是利用电解原理制备H3PO2的示意图;已知电极反应为:
阳极 4OH--4e→O2↑+H2O
阴极 2H++2e→H2↑):
分析在阳极室得到H3PO2原因:阳极反应中消耗水电离的OH-,使c(H+)增大,H2PO2-通过阴离子交换膜进入阳极室,得到产品.
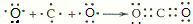 ;用电子式表示C、D两元素形成化学键的过程
;用电子式表示C、D两元素形成化学键的过程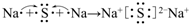 .
.