��Ŀ����
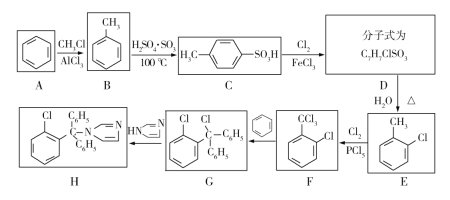
����Ŀ����ù��Ϊ�������ҩ���Զ�����������ǰ�ɫ��������нϺõĿ������ã���ϳ�·������ͼ��
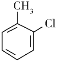
��֪���ױ������������Ȼ������µõ��������ʣ�![]() ��
�� �� �ش��������⣺
�� �ش��������⣺
(1)E��������______��F�еĹ���������Ϊ______��
(2)�ϳɿ�ù��Ĺ����У��������ķ�Ӧ������______��
(3)����B��ȡE�Ĺ����У�������Bһ����Ӧ����E����ԭ��Ϊ______��
(4)д��C��D�Ļ�ѧ����ʽ______��
(5)M��G��Ϊͬ���칹�壬������������������M��______��(������G����)
�ٺ�����������
�ڱ���֮�䲻ֱ������
д�����к˴Ź���������5��壬�ҷ������Ϊ2��2��1��1��1�Ľṹ��ʽ______��
(6)���������Ϣ��д���ñ�Ϊԭ�ϣ��Ʊ�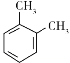 �ĺϳ�·��______(�����Լ���ѡ)��
�ĺϳ�·��______(�����Լ���ѡ)��
���𰸡����ȼױ� ��ԭ�� ȡ����Ӧ �ױ�ֱ�ӷ����ȴ���Ӧ�õ����ȼױ��Ͷ��ȼױ����Է��� 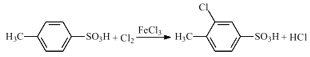 14
14 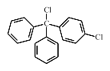
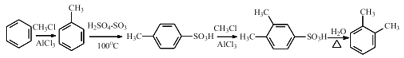
��������
������ͼ����֪��Ϣ��֪D�Ľṹ��ʽΪ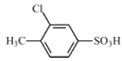 ���ٸ��ݸ����ʵĽṹ��ʽ���������ʷ����ƶϣ�ͬ���칹����дʱ���õ�Ч��ķ���д��ͬ���칹�塣
���ٸ��ݸ����ʵĽṹ��ʽ���������ʷ����ƶϣ�ͬ���칹����дʱ���õ�Ч��ķ���д��ͬ���칹�塣
��1��E�Ľṹ��ʽΪ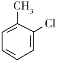 ������Ϊ���ȼױ���F�Ľṹ��ʽΪ
������Ϊ���ȼױ���F�Ľṹ��ʽΪ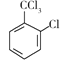 ��������Ϊ��ԭ�ӣ�
��������Ϊ��ԭ�ӣ�
�ʴ�Ϊ�����ȼױ�����ԭ�ӣ�
��2��A��BΪȡ����Ӧ��B��CΪȡ����Ӧ��C��DΪȡ����Ӧ��D��EΪˮ�ⷴӦ��ҲΪȡ����Ӧ��E��FΪȡ����Ӧ��F��GΪȡ����Ӧ��G��HΪȡ����Ӧ�������ķ�ӦΪȡ����Ӧ��
�ʴ�Ϊ��ȡ����Ӧ��
��3������֪��Ϣ��֪�ױ������������Ȼ������µõ��������ʣ�![]() ��
�� �����ȼױ��Ͷ��ȼױ����Է��룬
�����ȼױ��Ͷ��ȼױ����Է��룬
�ʴ�Ϊ���ױ�ֱ�ӷ����ȴ���Ӧ�õ����ȼױ��Ͷ��ȼױ����Է��룻
��4��C��D�Ļ�ѧ����ʽΪ�� ,
,
�ʴ�Ϊ�� ��
��
��5��M��G��Ϊͬ���칹�壬����ٺ������������ڱ���֮�䲻ֱ�������������������ض�����ͬһ̼ԭ���ϣ���һ�ȴ���������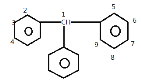 λ�÷ֱ�Ϊ1,2,3,4������ȴ�����14�֣�ȡ��λ�÷ֱ�Ϊ1��2��1,3��1,4��5,6��5,7��5,8��5��9��6��7��6,8��5,2��5,3��5,4��6,3��6,4��7,4����15�ֽṹ����ȥG����������14��ͬ���칹�壬���к˴Ź���������5��壬�ҷ������Ϊ2��2��1��1��1�Ľṹ��ʽΪ
λ�÷ֱ�Ϊ1,2,3,4������ȴ�����14�֣�ȡ��λ�÷ֱ�Ϊ1��2��1,3��1,4��5,6��5,7��5,8��5��9��6��7��6,8��5,2��5,3��5,4��6,3��6,4��7,4����15�ֽṹ����ȥG����������14��ͬ���칹�壬���к˴Ź���������5��壬�ҷ������Ϊ2��2��1��1��1�Ľṹ��ʽΪ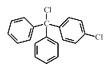 ��
��
�ʴ�Ϊ��14�� ��
��
��5��)���������Ϣ���ñ�Ϊԭ�ϣ��Ʊ�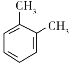 �ĺϳ�·��Ϊ��
�ĺϳ�·��Ϊ��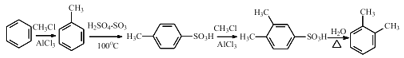 ��
��
�ʴ�Ϊ�� ��
��

����Ŀ����ѧ��Ӧ���ʺͻ�ѧ��Ӧ�����ǻ�ѧ��Ӧԭ������Ҫ��ɲ��֡�
(1)̽����Ӧ������0.10mol/LNa2S2O3��Һ��0.10mol/L ϡH2SO4��Ӧ���ʵ�Ӱ�졣��Ӧ����ʽΪ��Na2S2O3 +H2SO4=Na2SO4+S��+SO2��+H2O����Ʋⶨ������£�
��� | ��Ӧ�¶�/�� | Na2S2O3��Һ/mL | ��/mL | H2SO4��Һ/mL | �� |
�� | 25 | 10.0 | 0 | 10.0 | x |
�� | 25 | 5.0 | A | 10.0 | y |
�� | 0 | 10.0 | 0 | 10.0 | z |
������ʵ��٢���̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬��aΪ____________������ʵ����Ҫ���������������������������Ϊ____________��x��y��z�Ĵ�С��ϵ��____________��
(2)�������й㷺����;����ҵ�Ϻϳɰ��ķ�Ӧ��N2(g)+3H2(g)=2NH3(g).
����֪��
��ѧ�� | H-H | N��N | N-H |
����kJ/mol���Ͽ�1mol��ѧ������Ҫ�������� | 436 | 945 | 391 |
��ϳɰ����Ȼ�ѧ����ʽ��________________________________________��
������Ӧ��ʼʱN2��H2��NH3��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.1mol/L���ﵽƽ��ʱNH3Ũ�ȵķ�Χ��____________________��
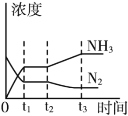
����ͼ��ʾ�÷�Ӧ��t1ʱ�̴ﵽ��ѧƽ�⣬��t2ʱ��ı�ij�������������仯���������t2ʱ�̸ı�����������__________��
����Ŀ���о�CO2��CH4��Ӧʹ֮ת��ΪCO��H2���Լ���ȼ��Σ���ͼ�������ЧӦ������Ҫ�����塣��ҵ��CO2��CH4������ӦI��CH4(g)+CO2(g)��2CO(g)+2H2(g) ��H1
�ڷ�Ӧ�����л�������Ӧ����H2(g)+CO2(g)��H2O(g)+CO(g)��H2=+41kJ/mol
(l)��֪���ֻ�ѧ���ļ����������±���ʾ��
��ѧ�� | C��H | H��H | C=O |
|
���ܣ�kJ/mol�� | 413 | 436 | 803 | 1076 |
����Hl =____kJ/mol����Ӧ����һ���������ܹ��Է����е�ԭ����____���÷�Ӧ��ҵ�������˵��¶Ⱥ�ѹǿΪ____�����ţ���
A.���¸�ѹ B�����µ�ѹ C�����¸�ѹ D�����µ�ѹ
(2)��ҵ�Ͻ�CH4��CO2�����ʵ���1:1Ͷ����ȡCO2��H2ʱ��CH4��CO2��ƽ��ת�������¶ȱ仯��ϵ��ͼ��ʾ��
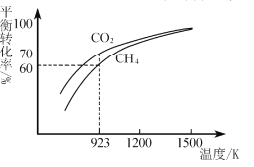
��923KʱCO2��ƽ��ת���ʴ���CH4��ԭ����________________________
�ڼ���923Kʱ��ӦII�Ļ�ѧƽ�ⳣ��K=______������������С�������λ����
��1200K����CO2��CH4��ƽ��ת����������ȵ�ԭ�������____��
(3)��ҵ��CH4��CO2��Ӧʱͨ�������O2������Ӧ
III: CH4+2O2��CO2+2H2O������O2��������Ӧ�����Ļ�̼�ͼ�С��Ӧ�����ȸ��ɣ���λʱ����ά�ַ�Ӧ�������蹩������������O2�Ľ������뷴Ӧ���ȸ��ɵĹ�ϵ��ͼ��ʾ��
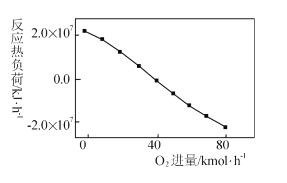
������O2�����������ӣ��ȸ����½���ԭ���� ____��
�ڲ���O2��ʹCH4��ƽ��ת����____������������������С����������������ͬ����CO2��ƽ��ת����________
����Ŀ����ΪԪ�����ڱ���һ���֣�����a-f�������ֶ���������Ԫ�أ����������գ�
a | b | c |
d | e | f |
(1)����Ԫ���У�ԭ�Ӱ뾶������_____________(��Ԫ�ر��)��
(2)��a����̬�⻯���ˮ��Һ�ʼ��ԣ���a����̬�⻯��ĵ���ʽ��________������Ԫ���У�����������Ӧˮ�����������ǿ����_________(��Ԫ�ط���)
(3)��fԪ�ص�ԭ��L���������M���������1������eԪ�صķǽ����Ա�fԪ�صķǽ�����___________(ѡ����ǿ����������)
(4)��bΪ�ǽ���Ԫ�أ��������ƶ���ȷ����___________(ѡ����)��
��aһ���ǽ���Ԫ�� ��dһ���ǽ���Ԫ�� ��fһ���Ƿǽ���Ԫ��