题目内容
【题目】下列不属于氧化还原反应的是
A.S+O2![]() SO2
SO2
B.4NH3+5O2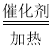 4NO+6H2O
4NO+6H2O
C.Na2SiO3+2HCl=H2SiO3(胶体)+2NaCl
D.2C12+2Ca(OH)2=Ca(C1O)2+CaCl2 +2H2O
【答案】C
【解析】
A.S+O2![]() SO2,反应前后S、O元素的化合价改变,该反应是氧化还原反应,A不符合题意;
SO2,反应前后S、O元素的化合价改变,该反应是氧化还原反应,A不符合题意;
B.4NH3+5O2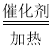 4NO+6H2O,反应前后N、O元素的化合价改变,该反应是氧化还原反应,B不符合题意;
4NO+6H2O,反应前后N、O元素的化合价改变,该反应是氧化还原反应,B不符合题意;
C.Na2SiO3+2HCl=H2SiO3(胶体)+2NaCl,该反应是复分解反应,反应前后元素化合价没有改变,该反应是非氧化还原反应,C符合题意;
D.2C12+2Ca(OH)2=Ca(C1O)2+CaCl2 +2H2O,反应前后C1元素的化合价改变,该反应是氧化还原反应,D不符合题意;
答案选C。

【题目】二氧化锰无论在实验室还是在生产、生活中均有广泛应用。工业上可以用制备对苯二酚的废液为原料生产二氧化锰。此工艺对节约资源、保护环境、提高经济效益有着重要意义。
(1)经分析知该废液中含有硫酸锰、硫酸铵、硫酸以及Fe2+、Co2+、Ni2+等金属离子。以此为原料制备化学二氧化锰的流程如图所示。
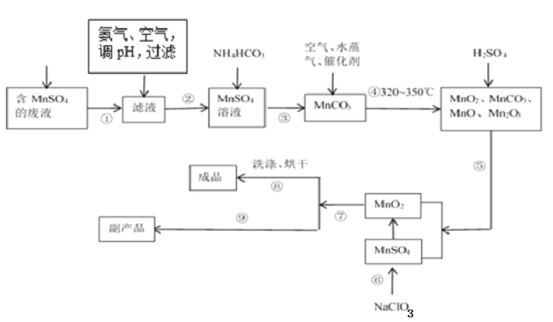
①常温下几种有关难溶硫化物的溶度积常数如下表,若除去Fe2+后的废液中Mn2+浓度为1mol/L,欲使Co2+和Ni2+完全沉淀,而Mn2+不受损失,S2-的浓度范围应控制在___mol/L。
化合物 | MnS | CoS(α型) | NiS |
Ksp | 2.5×10-10 | 4×10-21 | 1.07×10-21 |
②步骤⑥的化学方程式为___。
③步骤①~⑨中涉及到过滤的操作有___。(填序号)
④步骤⑨得到的副产品的化学式为___,其重要的用途之一是___。得到该副产品的操作是___。
(2)生产电解二氧化锰的原理是在93℃左右以石墨为电极电解硫酸锰和硫酸的混合溶液,写出阳极的电极反应式___,若电解过程中的电压为3V,理论上生产1tMnO2消耗电能___kw·h。(1kw·h=3.6×106J)
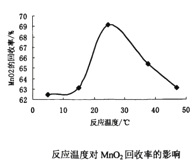
(3)双氧水氧化法制备二氧化锰时所发生的反应为MnSO4+2NH3+H2O2→MnO2+(NH4)2SO4,在溶液的pH、过氧化氢的用量和反应时间一定的情况下,温度对实验结果的影响如图所示。MnO2的回收率随着温度升高先增大后减小的可能原因是___。