题目内容
高铁酸钾(K2FeO4)具有很强的氧化性,在生产、生活中有广泛应用。
(1)K2FeO4常用做高效水处理剂,其两种作用分别是_____。
[已知:FeO42-+3e-+4H2O Fe(OH)3+5OH-]
Fe(OH)3+5OH-]
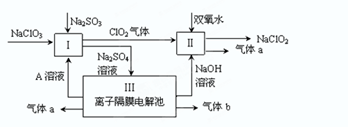
(2)制备K2FeO4可以采用湿式氧化法,流程如下图: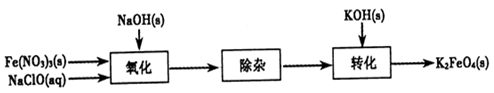
①完成氧化工序的离子方程式:
②除杂工序目的是除去Na2FeO4溶液中的杂质,除去的杂质主要有_____(写化学式)。
③转化工序控制在某温度下进行,则该温度下溶解度:Na2FeO4_____K2FeO4 (填“>”、“<”或“=”)。
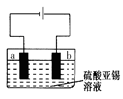
(3)实验室模拟工业电解法制取K2FeO4,装置如右图。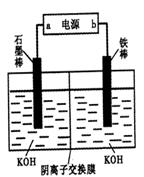
①此装置中电源的负极是____(填“a”或“b”)。
②阳极的电极反应式为______。
(4)已知K2FeO4稀溶液中存在如下平衡:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示:
4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示: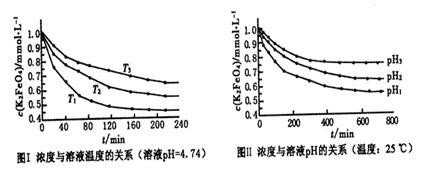
①由图I可得出的结论:该反应的△H___0(填“>”、“<”或“=”)。
②图Ⅱ中pH1___pH3(填“>”、“<”或“=”)。
(1)杀菌和凝聚 (2)①ClO2-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O
②NaNO3、NaCl ③> (3)①a ②Fe-6e-+8OH-=FeO42-+4H2O
(4)①> ②<
解析试题分析:(1)已知FeO42-+3e-+4H2O Fe(OH)3+5OH-,这说明K2FeO4具有强氧化性,能杀菌消毒。另外生成的铁离子水解生成氢氧化铁胶体具有吸附性,还起到净水剂的作用。
Fe(OH)3+5OH-,这说明K2FeO4具有强氧化性,能杀菌消毒。另外生成的铁离子水解生成氢氧化铁胶体具有吸附性,还起到净水剂的作用。
(2)①根据方程式可知,反应中氯元素的化合价从+1价降低到-1价,得到2个电子。铁的化合价从+3价升高到+6价,得到2个电子,因此根据电子得失守恒可知,氧化剂与还原剂的物质的量之比是3:2。由于溶液显碱性,所以根据原子守恒可知,反应后还有水生成,则该反应的离子方程式为3ClO2-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O。
②根据原子守恒可知,反应中还有硝酸钠和氯化钠生成,所以除杂的目的是除去NaNO3、NaCl。
③根据该温度下高铁酸钠能转化为高铁酸钾,所以根据沉淀容易向更难的方向转化可知,高铁酸钠的溶解度大于高铁酸钾的溶解度。
(3)①电解法制取K2FeO4,则反应中铁应该是失去电子,所以铁是阳极,因此b是电源的正极,a是大于的负极。
②铁是阳极失去6个电子,因此阳极电极反应式为Fe-6e-+8OH-=FeO42-+4H2O。
(4)①由图I可知,温度T1首先达到平衡状态,这说明温度T1最高。但温度高K2FeO4溶液浓度越小,这说明升高温度平衡向正反应方向移动,因此正方应是吸热反应,即该反应的△H>0。
②pH越小,溶液的酸性越强,则溶液中OH-越小,有利于平衡向正反应方向移动。所以根据图2可知pH1时K2FeO4溶液浓度最小,因此pH1小于pH3。
考点:考查高碳酸盐的作用、氧化还原反应方程式配平、溶解平衡、电解原理的应用以及外界条件对平衡状态的影响等

“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:(将配平后的系数填在横线上)
__ C+ __ KMnO4+ ___ H2SO4→___CO2↑+ ___MnSO4 + ___K2SO4+ ___H2O
当反应中有2.408×1024个电子发生转移时,还原剂的质量为
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)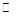 CO2(g)+H2(g),得到如下两组数据:
CO2(g)+H2(g),得到如下两组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | x | 2.0 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2.0 | 1.0 | 0.4 | 1.6 | 3 |
①实验1中以v(CO2)表示的反应速率为 (要求2位有效数字,下同);实验2达到平衡时CO的体积分数为 。
②若反应的平衡常数大,处理CO的效率高,则增大该反应平衡常数的措施有 。
③900℃时,该密闭容器中,加入4 molCO,3 mol H2O ,4mol CO2和2.4mol H2,比较此时正、逆反应速率的大小:v正 ______ v逆 (填“>”、“<”或“=”)。
④一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的有 。
A.容器中气体的平均分子量不随时间而变化
B.消耗1molH2的同时消耗1molCO
C.容器中气体的密度不随时间而变化
D.CO2的体积分数不随时间而变化
(3)汽车尾气的排放对空气造成污染。目前采用的是在汽车排气装置中安装一个净化器,可以有效将尾气中的有害气体转化。如:
①CO (g)+NO2(g) =CO2(g) + NO (g) ΔH =-a kJ/mol (a>0)
② 2CO (g)+2NO(g) =2CO2(g) )+ N2 (g) ΔH =-b kJ/mol (b>0)
若用标准状况下3.36LCO还原NO2至N2(CO完全反应)时放出的热量为 kJ(用含a和b的代数式表示,下同);并写出该反应的热化学方程式 。
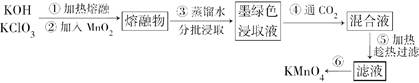
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
请同答下列问题:
(l)写出向KOH溶液中通入足量Cl2发生反应的离子方程式_______ 。
(2)在溶液I中加入KOH固体的目的是______(填编号)。
| A.为下一步反应提供碱性的环境 |
| B.使KClO3转化为KClO |
| C.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| D.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
(4)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:_______ FeO42-+_______ H2O="_______" Fe(OH)3(胶体)+_______O2↑+_______OH-。
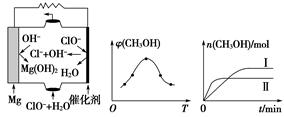
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示。电解过程中阳极的电极反应式为________。

(6)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:3Zn(OH)2+2Fe(OH)3+4KOH-----3Zn+2K2FeO4+8H2O,放电时电池的负极反应式为________ 。
 CH3OH(g)+H2O(g) ΔH。
CH3OH(g)+H2O(g) ΔH。