题目内容
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现
①Si(s)+3HCl(g)
SiHCl3(g)+H2(g) ②SiHCl3+H2
Si+3HCl
对上述两个反应的下列叙述中,错误的是( )
①Si(s)+3HCl(g)
| ||
| ||
对上述两个反应的下列叙述中,错误的是( )
| A、两个反应都是置换反应 |
| B、反应②不是置换反应 |
| C、工业上制得高纯硅可用于计算机芯片 |
| D、两个反应都是氧化还原反应 |
考点:硅和二氧化硅
专题:碳族元素
分析:一种化合物和一种单质反应生成另外的单质和化合物的反应为置换反应,与电子转移的化学反应是氧化还原反应,其特征是有元素化合价升降,据此分析解答.
解答:
解:A.这两个反应中都有单质和化合物参加和生成,所以都属于置换反应,故A正确;
B.反应②中有单质和化合物参加和生成,所以属于置换反应,故B错误;
C.硅具有金属和非金属的性质,是良好的半导体材料,在制作计算机芯片、太阳能电池的主要材料,故C正确;
D.两个反应中Si、H元素化合价都发生变化,所以都有电子转移,为氧化还原反应,故D正确;
故选B.
B.反应②中有单质和化合物参加和生成,所以属于置换反应,故B错误;
C.硅具有金属和非金属的性质,是良好的半导体材料,在制作计算机芯片、太阳能电池的主要材料,故C正确;
D.两个反应中Si、H元素化合价都发生变化,所以都有电子转移,为氧化还原反应,故D正确;
故选B.
点评:本题考查了基本概念,根据置换反应、氧化还原反应概念内涵来分析解答即可,注意:有单质参加和单质生成的反应不一定是置换反应,如同素异形体之间的转化,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
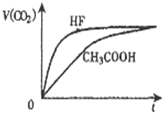 相同温度,浓度均为0.1mol/L,等体积的三种溶液:①HF溶液、②CH3COOH溶液、③NaHCO3溶液,已知将 ①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)的变化如图所示,下列说法正确的是( )
相同温度,浓度均为0.1mol/L,等体积的三种溶液:①HF溶液、②CH3COOH溶液、③NaHCO3溶液,已知将 ①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)的变化如图所示,下列说法正确的是( )| A、上述三种溶液中:c( OH-)大小:③>②>① |
| B、物质酸性的比较:CH3COOH>HF>H2CO3 |
| C、反应结束后所得两溶液中,c(CH3COO-)>c(F-) |
| D、①和 ③反应结束后所得溶液中:c(F-)+c(HF)═0.10mol/L |
下列关于同系物的说法中,错误的是( )
| A、同系物具有相同的分子式 |
| B、同系物符合同一通式 |
| C、相邻的同系物彼此在组成上相差一个CH2原子团 |
| D、同系物的化学性质基本相似 |
含硒(Se)的保健品已开始进入市场.已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是( )
| A、非金属性比硫强 |
| B、氢化物比HBr稳定 |
| C、处于金属与非金属的分界线上 |
| D、最高价氧化物的水化物为H2SeO4 |
下列属于物质化学变化的是( )
| A、结晶法除去NaCl中少量的KNO3 |
| B、气球充入过量的空气,爆炸 |
| C、金属钠有强还原性,能与水反应 |
| D、氯化氢溶于水生成盐酸 |
下列关于苯的同系物的命名说法中错误的是( )
| A、苯的同系物命名必须以苯作为母体,其他的基团作为取代基 |
| B、二甲苯可以以邻、间、对这种习惯方法进行命名 |
| C、二甲苯也可以用系统方法进行命名 |
| D、化学式是C8H10的苯的同系物有4种同分异构体 |
0.02mol氯化铬(CrCl3?6H2O)在水溶液中用过量的AgNO3处理,产生0.04mol AgCl沉淀,此氯化铬最可能形成的是( )
| A、[Cr(H2O)6]Cl3 |
| B、[Cr(H2O)3Cl3]?3H2O |
| C、[Cr(H2O)4Cl2]Cl?2H2O |
| D、[Cr(H2O)5Cl]Cl2?H2O |
要得到较大颗粒的明矾晶体,在结晶时可如下操作( )
| A、配制比室温高10~20℃明矾饱和溶液然后浸入悬挂的明矾小晶核,静置过夜 |
| B、在沸水中配制明矾饱和溶液,然后急速冷却结晶 |
| C、室温下,在明矾饱和溶液中投入明矾小晶核,静置过夜 |
| D、进行快速蒸发明矾饱和溶液至大量晶体析出 |
近年来,加“碘”食盐较多使用碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为KI+H2O→KIO3+H2↑(未配平).下列有关说法中,正确的是( )
| A、电解时,石墨做阴极,铁作阳极 |
| B、电解时,在阳极上产生氢气 |
| C、电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧 |
| D、电解中,每转移0.6mol电子,理论上可得到0.1mol无水KIO3晶体 |