题目内容
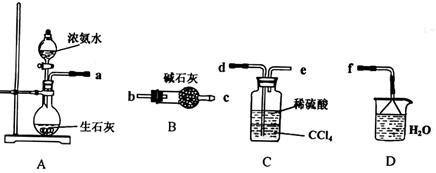
在金属冶炼和电子工业中,钙常作为空气的除气剂,以除去微量的氮氧气。一化学兴趣小组对金属钙在空气中燃烧的产物做了以下探究实验。取一定量的钙在空气中加热,使其充分燃烧,燃烧时火焰呈砖红色,燃烧后得白色固体M。将M研细后称取4.84g放入锥形瓶B中,滴加适量水使固体完全反应,通过下图测量生成的气体体积,进而推算白色固体的成分。
(1)用洁净铂丝蘸取CaCl2溶液在无色灯焰上灼烧,现象为__________。连接A和B的导气管的作用是___________________________,C中所加颗粒状固体是_______________。
(2)量气管D、E中应加的液体是_________。
A.水 B.四氯化碳 C.乙醇 D.盐酸
(3)实验中,B瓶壁发热。B中反应结束后,读取量气管中气体体积时,正确的操作为______________________。
(4)读取D中气体体积时,B、C中仍有少量产物气体,是否影响应该测得的气体体积__________________。
(5)若在D中得到气体448mL(已换算为标况),该气体有刺激性气味、能够使湿润的红色石蕊试纸变蓝,则4.84g固体M中的成分(填化学式)及其质量为________________。
(1)火焰呈砖红色;便于分液漏斗中的水顺利滴下来,提高氨气体积的测量精度;碱石灰。
(2)B
(3)冷至室温,D和E中液面相平,平视读数(答出2点即可)
(4)不影响
(5)1.48gCa3N2和3.36gCaO 。
解析试题分析:(1)钙元素焰色反应是砖红色,火焰呈砖红色。导气管连接A和B可以是分液漏斗上下气压相同,便于分液漏斗中的水顺利滴下来,以提高氨气体积的测量准确度。C中所加碱石灰目的是干燥氨气但又不消耗氨气。(2)量气管D、E中应加的四氯化碳,因为氨气能溶解在另外三种液体就不能准确量取气体体积了。(3)量气管中气体体积正确的操作是冷至室温、D和E中液面相平、,平视读数。(4)因为在反应前B、C中就有空气,故这时若B、C有少量气体时不会影响应该测得的气体体积。(5)空气的主要成分是N2、O2,Ca在空气中燃烧产物只可能生成是的CaO和Ca3N2一种或两种。白色固体M与水反应放出有刺激性气味、能够使湿润的红色石蕊试纸变蓝的气体是氨气,所以一定含Ca3N2,利用N守恒可求其质量,然后根据与白色固体M的质量差就可确定有无CaO及它的质量的多少。
【考点】考查金属钙、氨气的性质以及量气体体积应该注意的问题等知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
(1)“酸浸”中硫酸要适当过量,目的是①提高铁的浸出率,② 。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为 。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-,
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓,
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O。
①若SnCl2不足量,则测定的Fe3+量 (填“偏高”、“偏低”、“不变”,下同),
②若不加HgCl2,则测定的Fe3+量 。
(4)①可选用 (填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是 (用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。
请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化: ;
b.沉淀: ;
c.分离,洗涤;
d.烘干,研磨。
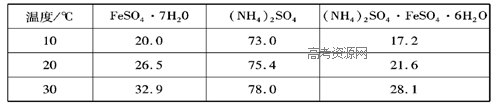
硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
| 实验次序 | 温度(℃) | 冷却后剩余固体的质量(g) |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
氯化钙常用于道路融冰剂和干燥剂,具有易溶于水,易吸潮等性质。实验室用工业大理石(含有少量Al2O3、Fe2O3等杂质)制备氯化钙的主要流程如下: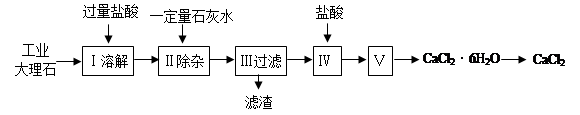 完成下列填空:
完成下列填空:
(1)上述使用的盐酸的物质的量浓度约为6.0mol/L,若用36.5%的盐酸(密度为1.2g/mL)配置6.0mol/L的盐酸100mL,所需的玻璃仪器有玻璃棒、量筒、胶头滴管、 ;需要量取36.5%的盐酸 mL;配制过程中,若其他操作都正确,下列操作会引起浓度偏小的是 。
| A.定容摇匀后发现液面低于刻度线 |
| B.定容时俯视容量瓶的刻度线 |
| C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就转入定容操作 |
| D.如果加水超过了刻度线,取出少量水使液面恰好到刻度线 |
(3)步骤Ⅱ控制石灰水用量的目的是防止(用离子方程式表示): 。
(4)滤渣的主要成分有(写化学式) 。
(5)步骤Ⅴ所含的操作依次是 、 。
(6)制得的氯化钙可以通过如下步骤测定其纯度:
①称取5.5g无水氯化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤;④ 、 ;⑤称量。若得到4.3g碳酸钙,则氯化钙的质量分数为 ;若实验操作规范而测定结果偏低,其原因是 。
以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
请回答下列问题:
(1)流程图中操作①、②、③分别指的是①_________、②__________、③________。
操作④、⑤用到的主要仪器是:④__________、⑤__________(每空填1-2个仪器)。
(2)判断溶液中SO42-离子已沉淀完全的方法是_________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,准确称取一定量的矿石试样,试样经溶解、预处理后,
| A.用带有刻度的烧杯配制成100 mL试样溶液。 | B.用量筒量取25.00 mL待测溶液, | C.并置于锥形瓶中。 | D.用蒸馏水洗涤滴定管后装入KMnO4标准溶液,用该标准溶液滴定待测试样,(E)当溶液变成淡紫红色时,停止滴定,如30秒内不褪色,(F)读取并计算滴定管中消耗的KMnO4标准溶液体积,计算试样中的Fe元素含量。请指出该实验过程中错误操作步骤的编号________________________。 |
(5)称取矿石试样1.60 g, 按方法Ⅰ分析,称得BaSO4的质量为4.66 g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是___________。
下列实验操作中错误的是( )
| A.过滤操作时如果有必要可以用蒸馏水洗涤滤纸上的沉淀2-3次 |
| B.蒸馏操作时,应使温度计水银球插入液态混合物中 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,萃取剂要和原溶剂互不相溶,且不能与溶质和溶剂反应 |