题目内容
6.下列变化或应用中,与分子间作用力有关的是( )| A. | 氯化钠晶体溶于水 | B. | 硝酸钾晶体的熔化、冷却 | ||
| C. | 次氯酸用于杀菌消毒 | D. | 夏天马路洒水降温 |
分析 A.氯化钠是离子晶体,微粒间的作用力是离子键;
B.硝酸钾是离子晶体,微粒间的作用力是离子键;
C.次氯酸用于杀菌消毒破坏化学键,与分子间作用力无关;
D.液态水吸热蒸发破坏分子间作用力.
解答 解:分子间作用力存在于分子晶体中,一般来说,分子晶体的状态发生改变时,分子间作用力发生变化.
A.氯化钠晶体溶于水,在水分子作用下电离出钠离子和氯离子,破坏的是离子键,故A错误;
B.硝酸钾晶体的熔化、冷却,破坏的是离子键,故B错误;
C.次氯酸中+1价的氯有强氧化性,可用于杀菌消毒,杀菌消毒时发生氧化还原反应生成-1价氯,破坏共价键,与分子间作用力无关,故C错误;
D.水属于分子晶体,液态水吸热蒸发降低周围环境温度,克服分子间作用力,故D正确;
故选D.
点评 本题考查晶体的结构与微粒间的作用力,注意把握晶体类型的判断以及粒子间作用力的区别,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
16.铝合金是制造飞机、汽车等的常用材料.下列关子${\;}_{13}^{27}$Al的叙述正确的是( )
| A. | 质子数是27 | B. | 中子数是27 | C. | 电子数是13 | D. | 质量数是13 |
1.某温度下,在0.1mol•L-1的NaHB强电解质溶液中,c(H+)>c(OH-),则下列关系式一定正确的是( )
| A. | .c(Na+)=c(HB-)+2c(B2-)+c(OH-) | B. | .c(Na+)=0.1mol•L-1≥c(B2-) | ||
| C. | .c(H+)•c(OH-)=10-14 | D. | 此溶液的pH=1 |
11.Li-SO2电池具有输出功率高和低温性能好等特点.其电解质是LiBr,溶剂是碳酸丙烯酯和乙腈,电池反应为2Li+2SO2$?_{充电}^{放电}$Li2S2O4.下列说法正确的是( )
| A. | 该电池反应为可逆反应 | |
| B. | 放电时,Li+向负极移动 | |
| C. | 充电时,阴极反应式为Li++e-═Li | |
| D. | 该电池的电解质溶液可以换成LiBr的水溶液 |
18.两种气态烃组成的混合物0.1mol,完全燃烧得0.16mol CO2和3.6g H2O,则混合物中( )
| A. | 一定有甲烷 | B. | 一定有甲烷和乙烯(C2H4) | ||
| C. | 可能有乙烷(C2H6) | D. | 一定有乙炔(C2H2) |
15.化合物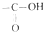 中的-OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看作酰卤的是( )
中的-OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看作酰卤的是( )
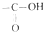 中的-OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看作酰卤的是( )
中的-OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看作酰卤的是( )| A. | CCl4 | B. | CH3COF | C. | CH3COCH2Cl | D. | CH2ClCOOH |
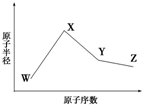 已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.
已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强.
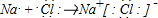
 A、B、C是单质,其中A是金属,各种物质间的转化关系如图所示.
A、B、C是单质,其中A是金属,各种物质间的转化关系如图所示.