题目内容
18.两种气态烃组成的混合物0.1mol,完全燃烧得0.16mol CO2和3.6g H2O,则混合物中( )| A. | 一定有甲烷 | B. | 一定有甲烷和乙烯(C2H4) | ||
| C. | 可能有乙烷(C2H6) | D. | 一定有乙炔(C2H2) |
分析 生成水的物质的量为:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.6H4,然后根据平均分子式进行判断.
解答 解:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.6H4.烃中C原子数小于1.6的只有甲烷,则一定含有甲烷,CH4分子中含4个氢原子,故另一种分子中一定含4个氢原子,且其碳原子数大于1.6,故可能是C2H4或C3H4等,一定没有C2H6或C2H2,二者的H原子不等于4,故A正确,BCD错误,故选A.
点评 考查有机物分子的推断,难度中等,关键是利用平均分子组成判断烃的组成,常用方法有:1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.可逆反应2A(g)?2B(g)+C(g)(吸热反应),达平衡后,要增大逆反应速率并使C的物质的量减少,可采取的措施有:①加压 ②加热 ③使用催化剂 ④增大B 浓度 ⑤增大A的浓度,上述措施中正确的是
( )
( )
| A. | 只有② | B. | 只有④ | C. | ①和④ | D. | ①和⑤ |
9.下列说法中,正确的是( )
| A. | 乙烯使溴水褪色,乙醇使酸性KMnO4溶液褪色,两者化学反应类型相同 | |
| B. | 1mol乙烯和Cl2完全加成后,再与Cl2彻底取代,两过程共消耗5mol Cl2 | |
| C. | 化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示 | |
| D. | 共价化合物中一定含有共价键,可能含有离子键 |
6.下列变化或应用中,与分子间作用力有关的是( )
| A. | 氯化钠晶体溶于水 | B. | 硝酸钾晶体的熔化、冷却 | ||
| C. | 次氯酸用于杀菌消毒 | D. | 夏天马路洒水降温 |
13.下列有关认识正确的是( )
| A. | 1s电子云呈球形,表示电子绕原子核做圆周运动 | |
| B. | 各能级的原子轨道数按s、p、d、f的顺序分别为1、3、5、7 | |
| C. | 各能层含有的能级数为n-1 (n代表能层序数) | |
| D. | 各能层含有的电子数为2n2(n代表能层序数) |
3.下列叙述正确的是( )
| A. | 苯、乙醇和乙酸都能发生取代反应 | |
| B. | 甲烷和Cl2反应与乙烯和溴的四氯化碳溶液反应属于同一反应类型 | |
| C. | 葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 | |
| D. | 苯不能使酸性KMnO4溶液褪色,因此苯不能发生氧化反应 |
10.小明体检的血液化验单中葡萄糖为5.9×10-3mmol/L.这里的“mmol/L”是指( )
| A. | 物质的量 | B. | 物质的量浓度 | C. | 质量百分含量 | D. | 物质的摩尔质量 |
8.某无色水溶液中能大量共存的离子组是( )
| A. | K+、Na+、CO32-、Cl- | B. | Ca2+、K+、CO32-、OH- | ||
| C. | Fe3+、Ba2+、NO3-、SO4- | D. | H+、Na+、HCO3-、OH- |
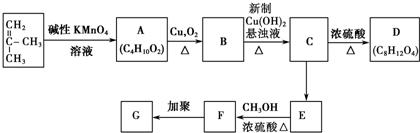
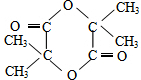 ,G的结构简式是
,G的结构简式是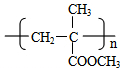 .
.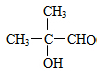 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$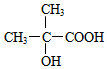 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.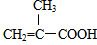 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.