题目内容
【题目】化合物H是一种著名的香料,某研究小组从苯出发,经两条路线合成化合物H。其中化合物D的分子式为C7H8 。
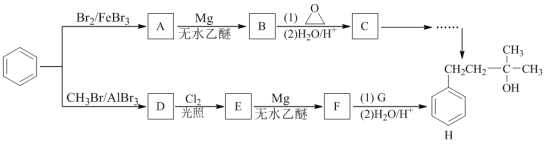
已知:I. RX+Mg无水乙醇R-MgX (X为卤素原子)
II. ![]()
III. 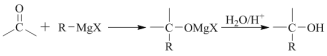
请回答:
(1)下列说法不正确的是________________________。
A.常温下,化合物A为褐色、密度比水大的液体
B.化合物C能发生消去反应
C.化合物D的一氯代物有4种
D.化合物E能发生水解反应和消去反应
(2)苯→D的化学方程式是___________________________________________。
(3)G的结构简式是_______________________________________。
(4)写出同时符合下列条件的C的所有同分异构体的结构简式________________________。
①能与FeCl3溶液发生显色反应;
②1H-NMR谱显示分子中含有四种不同环境的氢原子。
(5)设计以C和丙酮为原料制备H的合成路线(用流程图表示,无机试剂任选,且不超过四步)。_____
【答案】AD ![]()
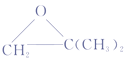
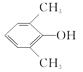 和
和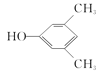
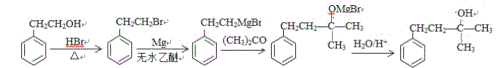
【解析】
根据从苯出发合成H的第一条路线,根据反应条件顺推可知,A为![]() ;结合已知信息中的反应条件顺推可知B为
;结合已知信息中的反应条件顺推可知B为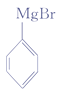 ;C为
;C为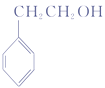 ;根据从苯出发合成H的第二条路线,根据反应条件顺推可知,D为
;根据从苯出发合成H的第二条路线,根据反应条件顺推可知,D为![]() ;E为
;E为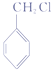 ;F为
;F为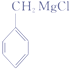 ;F到G增加了4个碳原子,根据G和H的结构特点以及反应条件,顺推可知G为
;F到G增加了4个碳原子,根据G和H的结构特点以及反应条件,顺推可知G为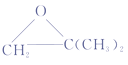 。
。
(1)A.常温下,化合物A(![]() )为无色油状、密度比水大的液体,选项A不正确;
)为无色油状、密度比水大的液体,选项A不正确;
B.化合物C为 ,能发生消去反应生成苯乙烯,选项B正确;
,能发生消去反应生成苯乙烯,选项B正确;
C.化合物D为![]() ,分子中有四种不同环境的氢原子,其一氯代物有4种,选项C正确;
,分子中有四种不同环境的氢原子,其一氯代物有4种,选项C正确;
D.化合物E为 ,在氢氧化钠的水溶液中能发生水解反应生成苯甲醇,但不能发生消去反应,选项D不正确;
,在氢氧化钠的水溶液中能发生水解反应生成苯甲醇,但不能发生消去反应,选项D不正确;
答案选AD;
(2)苯→D是苯与一溴甲烷发生取代反应生成甲苯和溴化氢,反应的化学方程式是![]() ;
;
(3)G的结构简式是 ;
;
(4) C为 ,其同分异构体,根据限定条件①能与FeCl3溶液发生显色反应可知存在酚羟基,根据限定条件②1H-NMR谱显示分子中含有四种不同环境的氢原子,可推出符合条件的同分异构体为
,其同分异构体,根据限定条件①能与FeCl3溶液发生显色反应可知存在酚羟基,根据限定条件②1H-NMR谱显示分子中含有四种不同环境的氢原子,可推出符合条件的同分异构体为 和
和 ;
;
(5)C为 ,与HBr反应制得
,与HBr反应制得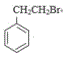 ,
, 在镁和无水乙醚中作用生成
在镁和无水乙醚中作用生成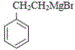 ,
, 与丙酮反应生成
与丙酮反应生成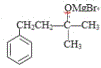 ,
, 酸化得到H的合成路线为
酸化得到H的合成路线为 。
。

 阅读快车系列答案
阅读快车系列答案【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
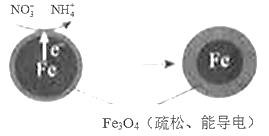
①作负极的物质是____。
②正极的电极反应式是____。
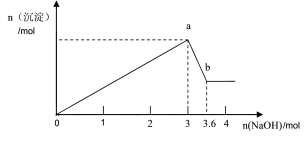
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
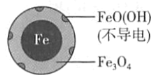
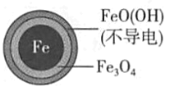
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是____。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____。
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。

①作负极的物质是____。
②正极的电极反应式是____。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是____。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____。