题目内容
锌锰干电池在放电时总反应方程式可以表示为:Zn(s)+2MnO2+2N Zn2++Mn2O3(s)+2NH3↑+H2O,在此电池放电时正极(碳棒)上发生反应的物质是( )
Zn2++Mn2O3(s)+2NH3↑+H2O,在此电池放电时正极(碳棒)上发生反应的物质是( )
| A.Zn | B.碳 | C.MnO2和N | D.Zn2+和NH3 |
C
解析

练习册系列答案
相关题目
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用右图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )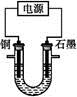
| A.铜电极连接电源正极 |
| B.黑色粉末X是铁粉 |
C.铜的相对原子质量的计算式是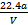 |
D.石墨电极上发生的反应是4OH--4e- O2↑+2H2O O2↑+2H2O |
下列是某校实验小组设计的一套原电池装置,下列有关描述不正确的是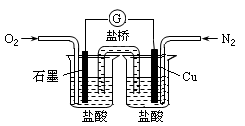
| A.此装置能将化学能转变为电能 |
| B.石墨电极的反应式:O2+2H2O+4e—=4OH— |
| C.电子由Cu电极经导线流向石墨电极 |
| D.电池总的反应是:2Cu+O2+4HCl=2CuCl2+2H2O |
电化学在日常生活中用途广泛,图甲是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是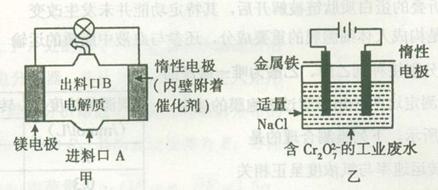
A.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2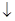 |
| B.图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| C.图乙电解池中,若有0.084 g阳极材料参与反应,则阴极会有336 mL的气体产生 |
| D.若图甲燃料电池消耗3.6 g镁产生的电量用以图乙废水处理,理论上可产生10.7 g氢氧化铁沉淀 |
一种新型污水处理装置如图所示。该装置可利用一种微生物将有机废水的化学能直接转化为电能。下列说法中不正确的是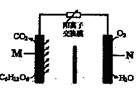
| A.电池工作时H+从M极区移向N极区 |
| B.N极为正极,发生还原反应 |
| C.M极的电极反应式为C6H12 O6 +6H2O-24e-=6CO2↑+24 H+ |
| D.当N极消耗5.6 L(标况下)气体时,则有2 NA个H+通过离子交换膜 |
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+ Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
| A.该装置可能是原电池,也可能是电解池 |
| B.该装置只能是原电池,且电解质溶液为硝酸 |
| C.该装置只能是电解池,且金属铜为该电解池的阳极 |
| D.该装置只能是原电池,电解质溶液不可能是盐酸 |
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )
| A.有O2放电的a极为电池的负极 |
| B.有H2放电的b极为电池的正极 |
C.a极对应的电极反应为O2+2H2O+4e- 4OH- 4OH- |
D.该电池的总反应方程式为2H2+O2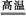 2H2O 2H2O |
如图所示,X为单质硅,Y为金属铁,a为NaOH溶液,组装成一个原电池,下列说法中正确的是( )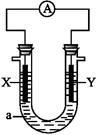
A.X为负极,电极反应为:Si-4e- Si4+ Si4+ |
B.X为正极,电极反应为:4H2O+4e- 4OH-+2H2↑ 4OH-+2H2↑ |
C.X为负极,电极反应为:Si+6OH--4e- Si+3H2O Si+3H2O |
D.Y为负极,电极反应为:Fe-2e- Fe2+ Fe2+ |
各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为( )。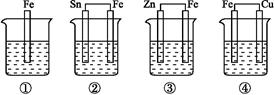
| A.②①③④ | B.④③①② | C.④②①③ | D.③②④① |