��Ŀ����
�绯ѧ���ճ���������;�㷺��ͼ����þһ��������ȼ�ϵ�أ�����ܷ�ӦΪ��Mg+ClO-+H2O=Cl-+Mg(OH)2 ��ͼ���Ǻ�Cr2O72-�Ĺ�ҵ��ˮ�Ĵ���������˵����ȷ����
��ͼ���Ǻ�Cr2O72-�Ĺ�ҵ��ˮ�Ĵ���������˵����ȷ����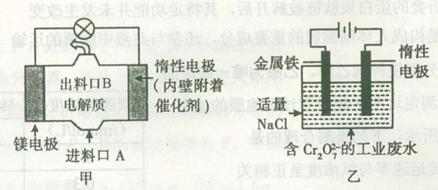
A��ͼ���з����Ļ�ԭ��Ӧ��Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2 |
| B��ͼ����Cr2O72-����Ե缫�ƶ�����ü�������OH-���ת����Cr(OH)3��ȥ |
| C��ͼ�ҵ����У�����0��084 g�������ϲ��뷴Ӧ������������336 mL��������� |
| D����ͼ��ȼ�ϵ������3��6 gþ�����ĵ�������ͼ�ҷ�ˮ�����������Ͽɲ���10��7 g������������ |
A
�������������A������ͼ��þһ��������ȼ�ϵ�صĽṹ��ClO?�������õ��ӣ�������ԭ��Ӧ��Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2 ����ȷ��B���������������������ƶ�������ͼ����Cr2O72-�������缫�ƶ�������C��ͼ�ҵ���������ӦΪFe��2e?=Fe2+��������ӦΪ2H++2e?=H2����������0��084 g�������ϲ��뷴Ӧ���������������������Ϊ��0.084g��56g/mol��22.4L/mol=0.0336L=33.6ml������D��ͼ��ȼ�ϵ������3��6 gþʱ��ʧȥ�ĵ���ʽ0.3mol��ͼ����������ӦΪ��Fe��2e?=Fe2+�����ݵ����غ㣬���ɵ�Fe2+Ϊ0.15mol������������ɵ�Fe(OH)3Ҳ��0.15mol������Ϊ16.05g������
����ȷ��B���������������������ƶ�������ͼ����Cr2O72-�������缫�ƶ�������C��ͼ�ҵ���������ӦΪFe��2e?=Fe2+��������ӦΪ2H++2e?=H2����������0��084 g�������ϲ��뷴Ӧ���������������������Ϊ��0.084g��56g/mol��22.4L/mol=0.0336L=33.6ml������D��ͼ��ȼ�ϵ������3��6 gþʱ��ʧȥ�ĵ���ʽ0.3mol��ͼ����������ӦΪ��Fe��2e?=Fe2+�����ݵ����غ㣬���ɵ�Fe2+Ϊ0.15mol������������ɵ�Fe(OH)3Ҳ��0.15mol������Ϊ16.05g������
���㣺���⿼��ԭ��ؼ�����ԭ����

��ͼ��ʾ��?Ϊֱ����Դ��?Ϊ�������Ȼ�����Һ�ͷ�̪��Һ����ֽ��?Ϊ��Ʋۡ���ͨ��·(δ�պ�K)����?�ϵ�c���Ժ�ɫ��Ϊʵ����Ƭ�϶�ͭ����ͨK��ʹc��d�����·��������������ȷ����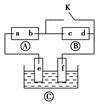
| A��bΪֱ����Դ�ĸ��� |
| B��f��Ϊ������������ԭ��Ӧ |
| C��e������Ϊ��Ƭ��f������ΪͭƬ |
| D����ѡ��CuSO4��Һ��CuCl2��Һ�����Һ |
��(N2H4)��������ȼ�ϵ����һ�ֻ����ͼ���ȼ�ϵ�أ������Ϊ20%~30%��KOH��Һ������ܷ�ӦΪN2H4+ O2=N2+2H2O�����й��ڸõ�ع���ʱ˵������ȷ����
| A����Һ��pH���ֲ��� |
| B����Һ�е��������������ƶ� |
| C�������ĵ缫��Ӧʽ��O2+4H++4e��=2H2O |
| D�������ĵ缫��Ӧʽ��N2H4+4OH����4e�� =4H2O +N2 |
ԭ������������������������Ź㷺Ӧ�á������й��ж��д������
װ�â� װ�â� װ�â�
| A��װ�â��о����ǵ��CuCl2��Һ��b�缫���к�ɫ�������� |
| B��װ�â��о����ǽ�����������ʴ��Fe�ϵķ�ӦΪFe��2e- = Fe2+ |
| C��װ�â��о����ǵ�ⱥ��ʳ��ˮ�� B�缫�����ķ�Ӧ��2Cl����2e- = Cl2�� |
| D������װ�����漰����Ҫ��Ӧ����������ԭ��Ӧ |
п�̸ɵ���ڷŵ�ʱ�ܷ�Ӧ����ʽ���Ա�ʾΪ:Zn(s)+2MnO2+2N Zn2++Mn2O3(s)+2NH3��+H2O,�ڴ˵�طŵ�ʱ����(̼��)�Ϸ�����Ӧ��������(����)
Zn2++Mn2O3(s)+2NH3��+H2O,�ڴ˵�طŵ�ʱ����(̼��)�Ϸ�����Ӧ��������(����)
| A��Zn | B��̼ | C��MnO2��N | D��Zn2+��NH3 |
��֪�����ڷŵ�ʱ��ԭ��ص�����,�ڳ��ʱ����ص����á��������õ�Ǧ��������һ���������״��Ǧ��Ǧ�����һ��ṹ���Ƶij���������Ǧ��Ǧ����ɡ������缫��ϡ�������������Һ���ڷŵ�ʱ,���������ķ�Ӧ�ɷֱ��ʾΪ:
Pb+S-2e- PbSO4
PbSO4
PbO2+4H++S+2e- PbSO4+2H2O
PbSO4+2H2O
���ʱ,���������ķ�Ӧ�ֱ��ʾΪ:
PbSO4+2e- Pb+S
Pb+S
PbSO4+2H2O-2e- PbO2+4H++S
PbO2+4H++S
�����طŵ�ʱ,��Һ��pH��(����)
| A������ | B������ | C������ | D����ȷ�� |
�õ�ⷨ��ȡ�Ȼ�ͭ��Һ�е�ͭ��������ȷ���ǣ� ��
| A����ͭƬ���ӵ�Դ����������һ�缫�ò�Ƭ |
| B����̼�����ӵ�Դ����������һ�缫��ͭƬ |
| C����������ͭ��Һ������������ |
| D���ô����ǵ�ľ�������������� |
ijС����������װ�ý��е绯ѧʵ�飬����ʵ�������Ԥ��������ȷ���ǣ� ��
| A��X��Y����������ӣ�������Cu������Zn�� |
| B��X��Y����������ӣ���Zn����Fe��õ������� |
| C��X��Y�ֱ����Դ����������������������Cu���������� |
| D��X��Y�ֱ����Դ����������������������Zn���������� |
���������Ǿ�����ǿ�����ˮ��Һ�ĵ������൱��һ�������塣�������ͨ�����е�����Ǩ�ƽ��е�ɴ��ݣ�����ֳ�Ϊ�������ӵ��塣Ŀǰ��������������ȫ��̬��ؼ�������������̽�����ȷ����Ӧ������㷺����RbAg4I5���壬����Ǩ�Ƶ�����ȫ��Ag�������µ����ʴ�0. 27 ����1��cm��1������RbAg4I5���壬�����Ƴɵ绯ѧ��������������ͼ��һ�ֲⶨO2���������崫����ʾ��ͼ����������O2���������ķ���ϩ��Ĥ���ɵ�ص綯�Ʊ仯���Ե�֪O2�ĺ����������崫�������������У����б仯�϶�û�з������ǣ� ��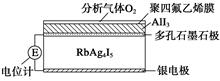
| A��I2��2Rb����2e��=2RbI |
| B��I2��2Ag����2e��=2AgI |
| C��Ag��e��=Ag�� |
| D��4AlI3��3O2=2Al2O3��6I2 |