��Ŀ����
����Ŀ���ס���ʵ��С���������ʵ��װ�÷ֱ��Ʊ�SnCl4��Ư�ۡ�
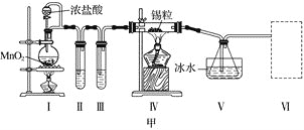
(1)��֪��a.�������۵�231 �棬��ѧ�������������ƣ�
b����������������ڽ�������Ӧ����SnCl4��SnCl4�ķе�114 ����
c��SnCl2��SnCl4����ˮ�⣬�������л��ܼ�����Sn2���ױ�����������ͼ��װ�ûش�
���Թܢ��е��Լ���____________________�����е��Լ���________________________��
�ڢ���װ�����ѡ��________(����ĸ)��
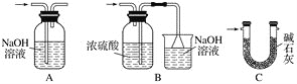
�ۢ�װ���з�Ӧ�����ӷ���ʽ��____________________________________________��
��ʵ�����������������װ�â���δ��Ӧ���MnO2����Ҫ�IJ���������______________��
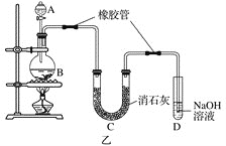
(2)��֪����Cl2�볱ʪ����ʯ�ҷ�Ӧ�Ƿ��ȷ�Ӧ�����¶Ƚϸ�ʱCl2�볱ʪCa(OH)2�ķ�ӦΪ6Cl2��6Ca(OH)2=Ca(ClO3)2��5CaCl2��6H2O��
����ͼ��װ�ûش𣺴�ʵ������Ca(ClO)2���ʽϵ͵�������
��________________________________________________________________________��
��________________________________________________________________________��
���𰸡�����ʳ��ˮ ŨH2SO4 C MnO2��4H����2Cl��![]() Mn2����Cl2����2H2O ��ͨ©�������������ձ� B��C֮��ȱ������HCl��װ�ã�2HCl��Ca(OH)2===CaCl2��2H2O Cl2����ʯ�ҷ�ӦΪ���ȷ�Ӧ���¶����ߣ�����Ca(OH)2ת��ΪCa(ClO3)2
Mn2����Cl2����2H2O ��ͨ©�������������ձ� B��C֮��ȱ������HCl��װ�ã�2HCl��Ca(OH)2===CaCl2��2H2O Cl2����ʯ�ҷ�ӦΪ���ȷ�Ӧ���¶����ߣ�����Ca(OH)2ת��ΪCa(ClO3)2
��������
(1) ��װ�â�����ȡ�����������Ȼ����ˮ�������������ᷴӦ����SnCl2��������SnCl4��ˮ�⣬�����Ʊ�SnCl4��Ҫ�ø��﴿��������������Ӧ��װ�â�������dz��Ӻ���ڸ���SnCl4��ˮ�⣬װ�â������ӵ�װ��Ӧ���и�����������������á��ۢ�װ���ж���������Ũ������������Ȼ��̡�������ˮ����MnO2������ˮ��ʵ��������ù��˷�����װ�â���δ��Ӧ���MnO2��(2)�����к��������Ȼ��⣬�Ȼ������������Ʒ�Ӧ�����Ȼ��ƣ�Cl2�볱ʪ����ʯ�ҷ�Ӧ�Ƿ��ȷ�Ӧ���¶����ߣ�Cl2�볱ʪCa(OH)2�ķ�ӦΪ6Cl2��6Ca(OH)2=Ca(ClO3)2��5CaCl2��6H2O��
(1) ��װ�â�����ȡ�����������Ȼ����ˮ�������������ᷴӦ����SnCl2��������SnCl4��ˮ�⣬�����Ʊ�SnCl4��Ҫ�ø��﴿��������������Ӧ��װ�â�������dz��Ӻ��װ�â���ʢ�ű���ʳ��ˮ����ȥ�����е��Ȼ��⣻װ�â���ʢ��ŨH2SO4��ȥ�����е�ˮ�������ڸ���SnCl4��ˮ�⣬װ�â������ӵ�װ��Ӧ���и�����������������ã���ѡC���ۢ�װ���ж���������Ũ������������Ȼ��̡�������ˮ����Ӧ�����ӷ���ʽ��MnO2��4H����2Cl��![]() Mn2����Cl2����2H2O����MnO2������ˮ��ʵ��������ù��˷�����װ�â���δ��Ӧ���MnO2����Ҫ�IJ�����������ͨ©�������������ձ���(2) �����к��������Ȼ�����B��C֮��ȱ������HCl��װ�ã�2HCl��Ca(OH)2===CaCl2��2H2O �� Cl2����ʯ�ҷ�ӦΪ���ȷ�Ӧ���¶����ߣ�Cl2�볱ʪCa(OH)2�ķ�ӦΪ6Cl2��6Ca(OH)2=Ca(ClO3)2��5CaCl2��6H2O������Ca(OH)2ת��ΪCa(ClO3)2��
Mn2����Cl2����2H2O����MnO2������ˮ��ʵ��������ù��˷�����װ�â���δ��Ӧ���MnO2����Ҫ�IJ�����������ͨ©�������������ձ���(2) �����к��������Ȼ�����B��C֮��ȱ������HCl��װ�ã�2HCl��Ca(OH)2===CaCl2��2H2O �� Cl2����ʯ�ҷ�ӦΪ���ȷ�Ӧ���¶����ߣ�Cl2�볱ʪCa(OH)2�ķ�ӦΪ6Cl2��6Ca(OH)2=Ca(ClO3)2��5CaCl2��6H2O������Ca(OH)2ת��ΪCa(ClO3)2��

 ��ҵ����ϵ�д�
��ҵ����ϵ�д�����Ŀ�����ڹ�ũҵ������Ӧ�ù㷺����ѹǿΪ30MPaʱ����ͬ�¶�ʱ�ϳɰ�ƽ����������NH3������������£�
�¶�/�� | 200 | 300 | 400 | 500 | 600 |
������/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
��ش�
��1������ͼ����ʾ���ϳɰ����Ȼ�ѧ����ʽΪ___��
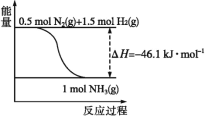
��2����1molN2(g)��3molH2(g)ͨ��һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������___92.2kJ(����������������������С����)��ԭ����___���������������H___(�������������С������������)��
��3����֪�ƻ�1molN��N����1molH��H����Ҫ���յ������ֱ�Ϊ946kJ��436kJ�����ƻ�1molN��H����Ҫ���յ�����Ϊ___kJ��
��4��N2H4����ΪNH3�����е�һ��H����NH2ȡ���IJ������������N2H4(g)Ϊȼ�ϣ���NO2Ϊ������������Ӧ����N2��H2O(g)��
��֪��N2(g)+2O2(g)=2NO2(g) ��H1=+67.7kJ��mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ��H2=-534kJ��mol-1��
��1molN2H4��NO2��ȫ��Ӧ���Ȼ�ѧ����ʽΪ___��
����Ŀ�����ֶ�����Ԫ�������ڱ��е����λ����ͼ��ʾ������ZԪ��ԭ�Ӻ��������������������������3������ش��������⣺
X | Y | |
Z | W |
(1)Ԫ��Zλ�����ڱ��е�____����____�塣
(2)X��YԪ���⻯���ȶ���ǿ��˳����____(�û�ѧʽ��ʾ)��
(3)Y��Z������������Ӧˮ���������ǿ��˳����____(�û�ѧʽ��ʾ)��
(4)ԭ��������Y��1��Ԫ�ص�һ���⻯���ֽܷ�Ϊ������һ���⻯��˷ֽⷴӦ�Ļ�ѧ����ʽ��____ ��


