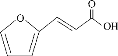
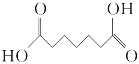
题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数为0.05NA
B.1 mol Na2O2与足量CO2和H2O充分反应,转移的电子数无法计算
C.m g CO与N2的混合气体中所含分子数目为![]() NA
NA
D.18 g 2H216O中含有的质子数与中子数均为10NA
【答案】C
【解析】
A.CH3COOH是弱酸, 0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数少于0.05NA,故A错误;
B.过氧化钠与二氧化碳或水的反应为歧化反应,1 mol Na2O2与足量CO2或水充分反应转移的电子数目为NA,故B错误;
C.CO与N2相对分子质量均为28,m g CO与N2的混合气体中所含分子数目为![]() NA,故C正确;
NA,故C正确;
D. 18 g 2H216O中含有的质子数为![]() ×10NA=9NA,中子数均为
×10NA=9NA,中子数均为![]() ×[(2-1)×2+(16-8)]NA=10NA,故D错误;
×[(2-1)×2+(16-8)]NA=10NA,故D错误;
故选C。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案【题目】某强酸性无色溶液中可能含下表离子中的若干种离子。
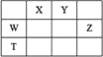
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO42- |
实验Ⅰ:取少量该强酸性溶液A进行如下实验。

实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液A,向该溶液中滴加1 mol·L-1的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
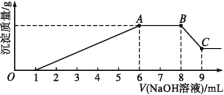
回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有________种。
(2)通过实验Ⅰ可以确定该溶液中一定存在的阴离子是_________。检验气体X的方法是_______________;沉淀Z的化学式为_____________。
(3)写出实验Ⅱ的图示中BC段对应反应的离子方程式:________________。
(4)A点对应的固体质量为____ g。
(5)通过上述信息,推算该溶液中阴离子的浓度为________ mol·L-1。