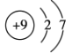题目内容
【题目】X、Y、Z、W为四种常见元素,其中X、Y、Z为短周期元素。有关信息如表所示.
原子或分子相关信息 | 单质或化合物相关信息 | |
X |
| X的最高价氧化物对应的水化物为无机酸中的最强酸 |
Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 |
Z | Z原子的最外层电子数是次外层电子数的 | Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 |
W | W原子的最外层电子数小于4 | W的常见化合价有 |
(1)W在周期表中的位置为______,![]() 在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为______
在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为______
(2)X的简单阴离子的结构示意图为______,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为________
(3)Z的氧化物在通讯领域用来作______,工业上制备Z的单质的化学反应方程式为______。锗与Z是同一主族元素,它可用来制造半导体品体管.研究表明:有机锗具有明显的抗肿瘤活性,锗不与![]() 溶液反应但在有
溶液反应但在有![]() 存在时可与
存在时可与![]() 溶液反应生成锗酸盐,反应的化学方程式为_______
溶液反应生成锗酸盐,反应的化学方程式为_______
【答案】第四周期Ⅷ族 4Fe(OH)2+O2+2H2O=4Fe(OH)3 ![]() Al2O3+6H+=2Al3++3H2O 光导纤维 SiO2+2C
Al2O3+6H+=2Al3++3H2O 光导纤维 SiO2+2C![]() Si+2CO↑
Si+2CO↑ ![]()
【解析】
X、Y、Z为短周期元素,X的最高价氧化物对应的水化物为无机酸中的最强酸,则X为Cl;Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料,Y原子的最外层电子数等于电子层数,则Y为Al;Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,原子的最外层电子数是次外层电子数的![]() ,则Z为Si;W原子的最外层电子数小于4,常见化合价有
,则Z为Si;W原子的最外层电子数小于4,常见化合价有![]() 、
、![]() ,
,![]() 的稀溶液呈黄色,则W为Fe。
的稀溶液呈黄色,则W为Fe。
(1)W为Fe,在周期表中的位置为第四周期Ⅷ族,![]() 在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。答案为:第四周期Ⅷ族;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。答案为:第四周期Ⅷ族;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)X的简单阴离子为![]() ,结构示意图为
,结构示意图为![]() ,X的最高价氧化物对应的水化物为高氯酸,Y的氧化物为氧化铝,二者反应的离子方程式为Al2O3+6H+=2Al3++3H2O。答案为:
,X的最高价氧化物对应的水化物为高氯酸,Y的氧化物为氧化铝,二者反应的离子方程式为Al2O3+6H+=2Al3++3H2O。答案为:![]() ;Al2O3+6H+=2Al3++3H2O;
;Al2O3+6H+=2Al3++3H2O;
(3)Z的氧化物为二氧化硅,在通讯领域用来作光导纤维,工业上制备硅单质的化学反应方程式为SiO2+2C![]() Si+2CO↑,锗不与
Si+2CO↑,锗不与![]() 溶液反应但在有
溶液反应但在有![]() 存在时可与
存在时可与![]() 溶液反应生成锗酸盐,反应的化学方程式为
溶液反应生成锗酸盐,反应的化学方程式为![]() 。答案为:光导纤维;SiO2+2C
。答案为:光导纤维;SiO2+2C![]() Si+2CO↑;
Si+2CO↑;![]() 。
。

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X(g)+3Y(g)2Z(g),其平衡常数为1600
C.改变温度可以改变此反应的平衡常数
D.改变压强,平衡常数不变,平衡不移动