题目内容
9.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 1L0.1mol/LNa2CO3溶液中,阴离子总数大于0.1NA | |
| B. | 常温常压下,1mol甘氨酸中含C-H键数目为3NA | |
| C. | 标准状况下,6.72LNO2与水充分反应转移电子数目为0.1NA | |
| D. | 50℃时,10LpH=13的NaOH溶液中含有的OH-数目为NA |
分析 A、碳酸根离子水解生成氢氧根离子和碳酸氢根离子;
B、根据甘氨酸的结构简式为:NH2-CH2-COOH来分析;
C、NO2与水的反应中,3molNO2转移2mol电子;
D、在50℃时,水的离子积Kw大于10-14.
解答 解:A、常温下,100mL 1mol•L-1 Na2CO3溶液中,碳酸根离子水解生成氢氧根离子和碳酸氢根离子,阴离子总数大于0.1NA,故A正确;
B、根据甘氨酸的结构简式为:NH2-CH2-COOH可知,1mol甘氨酸含2molC-H键,故B错误;
C、标准状况下,6.72 L NO2的物质的量n=$\frac{6.72L}{22.4L/mol}$=0.3mol,而NO2与水的反应中,3molNO2转移2mol电子,故0.3mol二氧化氮转移0.2mol电子,故C错误;
D、在50℃时,水的离子积Kw大于10-14,10 L pH=13的NaOH溶液中OH-的物质的量浓度不是0.1mol/L,故OH-数目不为NA,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
4.下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
| A. |  实验室制乙烯 | |
| B. | 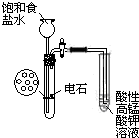 实验室制乙炔并验证乙炔发生氧化反应 | |
| C. | 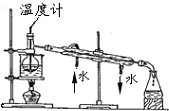 实验室中分馏石油 | |
| D. | 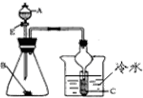 若A为稀硫酸、B为碳酸钠(粉状)、C为苯酚钠溶液,验证稀硫酸、苯酚、碳酸酸性的强弱 |
14.下列烃中可能存在同分异构体的是( )
| A. | 乙烷 | B. | 丙烷 | C. | 丁烷 | D. | 丙烯 |
1.分子式为C5H10O2的有机物A,有果香味,在酸性条件下水解生成有机物B和C,其中C能被催化氧化成醛,则A可能的结构共有( )
| A. | 1种 | B. | 6种 | C. | 9种 | D. | 18种 |
18.SO2有毒,但葡萄酒里都含有SO2,起保鲜、杀菌和抗氧化作用.下列说法不正确的是( )
| A. | 葡萄酒中的SO2对人体无害,是因为它的含量很少 | |
| B. | 葡萄酒中的SO2具有抗氧化作用,是因为它具有较强的还原性 | |
| C. | 从红葡萄酒的颜色判断,其中的SO2没有漂白性 | |
| D. | 葡萄酒倒入酒杯摇一摇,可以减少其中SO2的含量 |
19.下列说法中错误的是( )
| A. | NH4H的电子式为: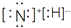 | B. | S2-的离子结构示意图为: | ||
| C. | H2O的形成过程: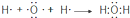 | D. | NaCl的形成过程: |
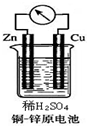 如图所示的铜-锌原电池中,理论上应观察到的现象是:
如图所示的铜-锌原电池中,理论上应观察到的现象是: