题目内容
4.已知酯在金属钠存在下与乙醇混合加热蒸馏,可使酯还原成醇,反应为RCOOR'+4[H]$\stackrel{Na+CH_{3}CH_{2}OH}{→}$RCH2OH+R'OH,现有酯C5H11COOC6H13,用上述方法还原,所得到的产物是( )| A. | C6H13OH和C5H11OH | B. | C6H13OH | ||
| C. | C5H11OH | D. | C11H23OH |
分析 依据题给信息:RCOOR'+4[H]$\stackrel{Na+CH_{3}CH_{2}OH}{→}$RCH2OH+R'OH,得出酯的还原产物分别是两种醇,且断键位置为酯基中的C-O单键,据此解答即可.
解答 解:由所给信息可知:酯的还原产物分别是两种醇,且断键位置为酯基中的C-O单键,那么C5H11COOC6H13,用上述方法还原应分别得到C5H11CH2OH和C6H13OH,即为己醇,故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、习题中的信息为解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.现有A、B、C、D、E五种易溶于水的强电解质,它们由如下离子组成(各种离子不重复).
已知:ⅰ0.1mol/L A溶液的pH<1;ⅱ将B溶液分别与其它四种溶液混合,均有白色沉淀产生;ⅲC溶液$→_{稀HNO_{3}}^{AgNO_{3}溶液}$白色沉淀.某同学根据以上实验得出如下结论:①A一定为H2SO4 ②B一定为Ba(OH)2 ③C可能是AlCl3 ④D、E两种物质中必有一种是NH4HCO3.以上说法中正确的个数是( )
| 阳离子 | H+、NH4+、Mg2+、Ba2+、Al3+ |
| 阴离子 | OH-、Cl-、HCO3-、NO3-、SO42- |
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
15.下列盛放物质的方法错误的是( )
| A. | 将金属钠保存在煤油中 | |
| B. | 液溴盛放在棕色细口的玻璃瓶中,加一些水,并密封置于低温处 | |
| C. | 碘化银盛放在无色玻璃瓶中,塞紧玻璃塞 | |
| D. | 新制的氯水盛放在棕色细口瓶中,塞紧玻璃塞 |
12.我国三峡工程每年所提供的电能,相当于一个每年燃烧3000万吨原煤的火力发电厂所产生的电能.因此建设三峡工程与建火力发电厂相比,有助于控制( )
①温室效应 ②硫的氧化物排放 ③白色污染 ④碳氢化合物排放.
①温室效应 ②硫的氧化物排放 ③白色污染 ④碳氢化合物排放.
| A. | ①④ | B. | ①② | C. | ②③ | D. | ③④ |
19.下列实验装置或操作正确的是( )
| A. | 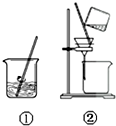 除去附着在铁屑表面的铝 | B. |  实验室制取乙酸乙酯 | ||
| C. |  实验室制乙烯 | D. |  分离酒精和水 |
9.下列有关说法中正确的是( )
| A. | 从组成元素上可以区别纯净物和混合物 | |
| B. | 碱性氧化物一定是金属氧化物 | |
| C. | 通过化学变化可以实现16O与18O问的相互转化 | |
| D. | 鸡蛋清溶液中加入饱和(NH4)2SO4溶液生成白色沉淀,属于化学变化 |
16.常温下,下列溶液中与1×10-5mol/L的NaOH溶液pH相同的是( )
| A. | 把pH=6的盐酸稀释1000倍 | |
| B. | 把pH=8的NaOH溶液稀释10倍 | |
| C. | 把10mL 1×10-5mol/L的H2SO4溶液与10mL 4×10-5mol/L的NaOH溶液相混合 | |
| D. | 把c(OH-)=10-5mol/L的NaOH溶液10mL加到100mL浓度为10-4mol/L的NaOH溶液中 |
13.化学知识广泛应用于生产生活中,下列叙述正确的是( )
| A. | 空气中的臭氧对人体健康有益无害 | |
| B. | 液氯罐泄漏时,可将其移入水塘中并加入生石灰 | |
| C. | 工业用食盐水制取氯气过程中,不涉及氧化还原反应 | |
| D. | 日常生活中物体能够热胀冷缩是因为构成物质的微粒能够热胀冷缩 |
14.以下事实不能用化学平衡移动原理解释的是( )
| A. | 夏天打开啤酒瓶,有大量气泡逸出 | |
| B. | 对于反应I2(g)+H2(g)?2HI(g)达到平衡后,增大压强气体颜色加深 | |
| C. | 紫色CoCl2溶液,加热溶液颜色变为蓝色,用冰水冷却溶液颜色变为粉红色 | |
| D. | 工业合成氨(N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol)选择高压条件 |