题目内容
14.现有A、B、C、D、E五种易溶于水的强电解质,它们由如下离子组成(各种离子不重复).| 阳离子 | H+、NH4+、Mg2+、Ba2+、Al3+ |
| 阴离子 | OH-、Cl-、HCO3-、NO3-、SO42- |
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 0.1mol/LA溶液的pH<1,说明氢离子浓度>0.1mol/L,为二元酸,所以A为硫酸;将B溶液分别与其它四种溶液混合,均有白色沉淀生成,可知B为氢氧化钡;氢氧化钡和硫酸反应生成硫酸钡沉淀,氢氧化钡和氯化镁或氯化铝或硝酸铝反应生成氢氧化镁或氢氧化铝沉淀,氢氧化钡和碳酸氢铵反应生成碳酸钡沉淀,由C溶液$→_{稀HNO_{3}}^{AgNO_{3}溶液}$白色沉淀,可知C含氯离子,C可能为氯化镁或氯化铝,氢氧化钡和氯化镁或氯化铝反应生成氢氧化镁或氢氧化铝沉淀,硝酸铵和氢氧化钡不生产沉淀,故硝酸根离子和Mg2+或Al3+结合成硝酸铝或硝酸镁,能和氢氧化钡生成沉淀,因此HCO3-只能和NH4+结合,碳酸氢铵和氢氧化钡反应生成碳酸钡沉淀,故D、E两种物质中必有一种是碳酸氢铵;要确定C的组成,即确定C为氯化镁还是氯化铝,即检验是否含镁离子还是铝离子,根据和氢氧化钠反应的现象来确定,据此答题.
解答 解:0.1mol/LA溶液的pH<1,说明氢离子浓度>0.1mol/L,为二元酸,所以A为硫酸;将B溶液分别与其它四种溶液混合,均有白色沉淀生成,可知B为氢氧化钡;氢氧化钡和硫酸反应生成硫酸钡沉淀,氢氧化钡和氯化镁或氯化铝或硝酸铝反应生成氢氧化镁或氢氧化铝沉淀,氢氧化钡和碳酸氢铵反应生成碳酸钡沉淀,由C溶液$→_{稀HNO_{3}}^{AgNO_{3}溶液}$白色沉淀,可知C含氯离子,C可能为氯化镁或氯化铝,氢氧化钡和氯化镁或氯化铝反应生成氢氧化镁或氢氧化铝沉淀,硝酸铵和氢氧化钡不生产沉淀,故硝酸根离子和Mg2+或Al3+结合成硝酸铝或硝酸镁,能和氢氧化钡生成沉淀,因此HCO3-只能和NH4+结合,碳酸氢铵和氢氧化钡反应生成碳酸钡沉淀,故D、E两种物质中必有一种是碳酸氢铵;要确定C的组成,即确定C为氯化镁还是氯化铝,即检验是否含镁离子还是铝离子,根据和氢氧化钠反应的现象来确定,
根据上面的分析可知,①A一定为H2SO4,正确; ②B一定为Ba(OH)2,正确; ③C可能是AlCl3,正确; ④D、E两种物质中必有一种是NH4HCO3,正确;即四个说法都正确,
故选D.
点评 本题考查了离子的推断,难度较大,要结合实验现象和离子的共存及题给信息综合判断.掌握物质之间的反应及离子的检验是关键.

 已知:25℃时某些弱酸的电离平衡常数(如表),如图图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化,下列说法正确的是
已知:25℃时某些弱酸的电离平衡常数(如表),如图图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化,下列说法正确的是| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=4.7×10-11 |
| A. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 图象中a、c两点处的溶液中$\frac{c(HR)×c(O{H}^{-})}{c({R}^{-})}$相等(HR代表CH3COOH或HClO) | |
| D. | 图象中a点酸的总浓度大于b点酸的总浓度 |
| A. | 氢氧化亚铁溶于稀硝酸:Fe(OH)2+2H+═Fe2++2H2O | |
| B. | 醋酸与NaHCO3溶液反应:H++HCO3-═CO2↑+H2O | |
| C. | 向KI溶液中加入FeCl3溶液:Fe3++2I-═Fe2++I2 | |
| D. | 将铝片加入烧碱溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| A. | 1:1:1 | B. | 6:3:2 | C. | 4:3:2 | D. | 6:4:3 |
| A. | 盐 | B. | 氧化物 | C. | 单质 | D. | 有机物 |
| A. | 10s | B. | 8s | C. | 大于10s | D. | 小于10s |
| A. | C6H13OH和C5H11OH | B. | C6H13OH | ||
| C. | C5H11OH | D. | C11H23OH |
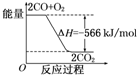 某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、S、NOX等进行研究具有重要意义.为减少SO2的排放,常采取的措施是:将煤转化为清洁气体燃料.涉及的化学反应为:
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、S、NOX等进行研究具有重要意义.为减少SO2的排放,常采取的措施是:将煤转化为清洁气体燃料.涉及的化学反应为: