题目内容
18.已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+ MnO4-→Mn2+ Cr2O72-→Cr3+ HNO3→NO
如果分别用上述这些物质氧化KI得到等量的I2,消耗物质的量最少的物质是( )
| A. | Fe3+ | B. | MnO4- | C. | Cr2O72- | D. | HNO3 |
分析 氧化还原反应中得失电子守恒,1mol氧化剂得电子越多,氧化KI得到等量的I2时消耗的物质的量越少;分别计算出1mol各离子发生反应得到的电子的物质的量,得到电子越多,则消耗的其物质的量越少.
解答 解:氧化还原反应中得失电子守恒,1mol氧化剂得电子越多,氧化KI得到等量的I2时消耗的物质的量越少,
A.1molFe3+→Fe2+得1mole-;
B.1molMnO4-→Mn2+得5mole-;
C.1molCr2O72-→Cr3+得6mole-;
D.1molHNO3→NO得1mole-;
根据分析可知,分别用上述这些物质氧化KI得到等量的I2,消耗物质的量最少的物质是Cr2O72-,
故选C.
点评 本题考查氧化还原反应的计算,为高频考点,题目难度中等,明确元素化合价的变化、电子守恒为解答的关键,试题侧重考查学生的分析与计算能力.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
8.下列实验操作中,正确的是( )
| A. | 用铂丝蘸取少量KCl溶液置于火焰上灼烧,直接观察火焰颜色,检验K+的存在 | |
| B. | 在蒸馏装置中,将温度计水银球插入液面以下 | |
| C. | 取绿豆大小的钠,研成粉末,放入装满水的烧杯,观察钠与水反应 | |
| D. | 用热的纯碱溶液洗去试管内壁附着的油脂 |
9.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,22.4L的H2O含NA个水分子 | |
| B. | 1.8g的NH4+离子中含有的电子数为 NA | |
| C. | 5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA个 | |
| D. | 常温常压下,32g臭氧和氧气的混合物含有的氧原子数为 NA |
13.下列反应的离子方程式正确的是( )
| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铝片插入硝酸汞溶液中:Al+Hg2+=Al3++Hg | |
| C. | Ba(OH)2与稀H2SO4反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 盐酸除铁锈:O2-+2H+═H2O |
7.用1L 1mol•L-1NaOH溶液吸收0.8molCO2,所得溶液中n(Na2CO3)和n(NaHCO3)之比约为( )
| A. | 1:3 | B. | 3:1 | C. | 2:3 | D. | 3:2 |
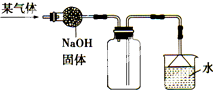 如图是收集某气体的装置.由实验装置推测该气体的有关性质可能正确的是( )
如图是收集某气体的装置.由实验装置推测该气体的有关性质可能正确的是( )