题目内容
8.1-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下: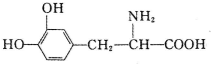
下列关于L-多巴性质的叙述.正确的是( )
| A. | 常温下,不溶于水 | B. | 既可与酸反应,又可与碱反应 | ||
| C. | 遇FeCl3溶液无变化 | D. | 与溴水混合,溴水褪色,溶液分两层 |
分析 该物质中含有酚羟基、苯环、氨基和羧基,具有酚、苯、氨基酸的性质,能发生氧化反应、取代反应、加成反应、缩聚反应、酯化反应等,据此分析解答.
解答 解:A.该物质中含有酚羟基、氨基、羧基能亲水基,能溶于水,故A错误;
B.含有酚羟基和羧基、氨基,所以具有两性,能与酸、碱发生反应,故B正确;
C.含有酚羟基,所以能与氯化铁溶液发生显色反应,故C错误;
D.与溴水混合时,与溴水发生取代反应生成沉淀,且该物质易溶于水,所以与水不分层,故D错误;
故选B.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系即可解答,侧重考查酚、氨基酸的性质,注意该物质中含有亲水基而易溶于水,题目难度不大.

练习册系列答案
相关题目
18.下列物质能用铝制器皿盛放的是( )
| A. | 稀硝酸 | B. | 稀硫酸 | C. | 浓硝酸 | D. | 浓盐酸 |
19.图所示装置中,已知电子由b极沿导线流向锌.下列判断正确的是( )
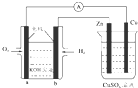

| A. | 该装置中Zn极为阳极 | |
| B. | 一段时间后铜片上质量增加 | |
| C. | a极反应的电极反应式为:O2+4e-+2H2O═4OH- | |
| D. | 当铜极的质量变化为32g时,b极上消耗的O2的体积为11.2 L |
16.通过下列方法测定1.80g金属Sn样品的纯度.
①将样品溶于盐酸:Sn+2HCl═SnCl2+H2↑;
②加过量FeCl3溶液:SnCl2+2FeCl3═SnCl4+2FeCl2;
③再用酸性KMnO4反应生成的Fe2+,用去0.1000mol/L的KMnO4溶液60.00mL,反应的离子方程式为:MnO4-+
5Fe2++8H+═Mn2++5Fe3++4H2O.
计算金属Sn样品的纯度为( )
①将样品溶于盐酸:Sn+2HCl═SnCl2+H2↑;
②加过量FeCl3溶液:SnCl2+2FeCl3═SnCl4+2FeCl2;
③再用酸性KMnO4反应生成的Fe2+,用去0.1000mol/L的KMnO4溶液60.00mL,反应的离子方程式为:MnO4-+
5Fe2++8H+═Mn2++5Fe3++4H2O.
计算金属Sn样品的纯度为( )
| A. | 99.2% | B. | 49.6% | C. | 96.2% | D. | 46.6% |
13.下列排列顺序中,错误的是( )
| A. | 原子半径:O<S<Na | B. | 稳定性:PH3>H2S>NH3 | ||
| C. | 电负性:P<S<Cl | D. | 第一电离能:Na<Al<Mg |
20.互为同分异构体的一组是( )
| A. | ${\;}_1^1$H与${\;}_1^2$H | B. | O2与O3 | C. | 乙醇与二甲醚 | D. | 甲烷与丁烷 |
17.下列装置或操作能达到实验目的是( )
| A. |  验证反应的热效应 | B. |  定量测定化学反应速率 定量测定化学反应速率 | ||
| C. |  滴定法测FeSO4溶液的浓度 | D. | 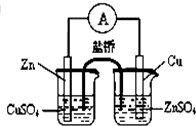 构成铜锌原电池 |
 某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题:
某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题:
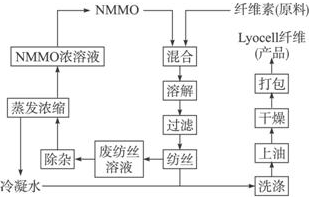

 .
. .
. .
.