题目内容
【题目】亚氯酸钠(NaClO2)是一种重要的杀菌消毒剂,同时也是对烟气进行脱硫、脱硝的吸收剂。
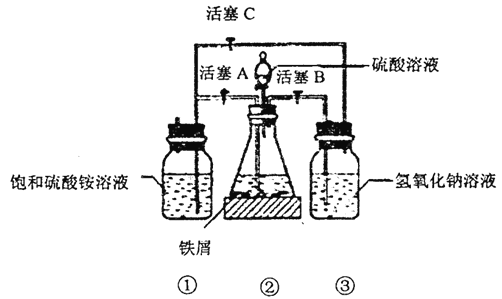
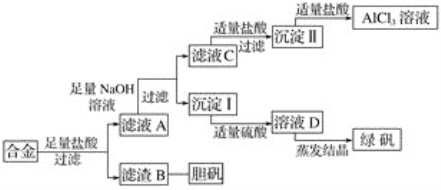
Ⅰ.以氯酸钠(NaClO3)为原料制备NaClO2粗品的工艺流程如下图所示:

已知:
i.纯ClO2易分解爆炸,空气中ClO2的体积分数在10%以下比较安全;
ii.NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解;
iii.NaClO2饱和溶液在温度低于38℃时析出NaClO23H2O,等于或高于38℃时析出NaClO2晶体,高于60℃时分解成NaClO3和NaCl。
(1)试剂A应选择_________。(填字母)
a.SO2 b.浓硝酸 c.KMnO4
(2)反应②的离子方程式为_________。
(3)已知压强越大,物质的沸点越高。反应②结束后采用“减压蒸发”操作的原因是________。
(4)下列关于上述流程的说法中,合理的是_________。(填字母)
a.反应①进行过程中应持续鼓入空气
b.反应①后得到的母液中,溶质的主要成分是NaCl
c.反应②中NaOH溶液应过量
d.冷却结晶时温度选择38℃,过滤后进行温水洗涤,然后在低于60℃下进行干燥,得到粗产品NaClO2
Ⅱ.采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。
(5)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol/L。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c /(mol/L) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_________。
②由实验结果可知,脱硫反应速率_________(填“大于”或“小于”)脱硝反应速率。除SO2和NO在烟气中的初始浓度不同外,还可能存在的原因是_________。(答出两条即可)
【答案】 a 2OH + 2ClO2 + H2O2 ![]() 2ClO2 + O2 + 2H2O 减压可以使物质沸点降低,实验较低温度下进行蒸发,可避免NaClO2因温度高而发生分解 acd 4OH +3ClO2 + 4NO
2ClO2 + O2 + 2H2O 减压可以使物质沸点降低,实验较低温度下进行蒸发,可避免NaClO2因温度高而发生分解 acd 4OH +3ClO2 + 4NO ![]() 4NO3 + 3Cl + 2H2O 大于 SO2比NO溶解度更大;在此条件下SO2还原性更强;脱硝反应活化能更大
4NO3 + 3Cl + 2H2O 大于 SO2比NO溶解度更大;在此条件下SO2还原性更强;脱硝反应活化能更大
【解析】NaClO3和浓H2SO4在反应器①中发生还原反应生成ClO2和Na2SO4,所以试剂A可以用二氧化硫, ClO2在反应器②中与双氧水、氢氧化钠反应生成亚氯酸钠,再得到其晶体。
(1)根据上面的分析可以知道试剂A为SO2,故选a,因此,本题正确答案是:a。
(2)反②中ClO2被双氧水还原成ClO2,反应的离子方程式为2OH+2ClO2+H2O2 ![]() 2ClO2+O2+2H2O , 因此,本题正确答案是: 2OH + 2ClO2 + H2O2
2ClO2+O2+2H2O , 因此,本题正确答案是: 2OH + 2ClO2 + H2O2 ![]() 2ClO2+ O2 + 2H2O
2ClO2+ O2 + 2H2O
(3)含水的NaClO2受热易分解,所以亚氯酸钠溶液中获得晶体,温度不能太高,所以反应②结束后采用“减压蒸发”操作,在较低温度蒸发浓缩,可防止温度过高.NaClO2分解。因此,本题正确答案是:在较低温度蒸发浓缩,可防止温度过高.NaClO2分解。
(4)根据信息纯ClO2易分解爆炸,空气中ClO2的体积分数在10![]() 以下比较安全,所以要持续通过量的空气, NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解,所以反应②中碱要过量,因为试剂A为二氧化硫, NaClO3被还原成ClO2,所以反应①后得到的母液中,溶质的主要成分是, Na2SO4。故选acd,因此,本题正确答案是:acd。
以下比较安全,所以要持续通过量的空气, NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解,所以反应②中碱要过量,因为试剂A为二氧化硫, NaClO3被还原成ClO2,所以反应①后得到的母液中,溶质的主要成分是, Na2SO4。故选acd,因此,本题正确答案是:acd。
(5) ①亚氯酸钠具有氧化性,且NaClO2溶液呈碱性,则NaClO2溶液脱硝过程中主要反应的离子方程式![]() ;因此,本题正确答案是:
;因此,本题正确答案是:![]() 。
。
②由实验结果可以知道,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率.原因是除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高, 因此,本题正确答案是:大于;NO溶解度较低或脱硝反应活化能较高。

【题目】化学反应的快慢和限度对人类生产、生活有重要的意义。
(1)将影响化学反应速率的因素镇在空格处。
实例 | 影响因素 |
食物放在冰箱里延长保质期 | ①___ |
实验室将块状药品研细,再进行反应 | ②___ |
(2)某小组将酸性KMnO4溶液与H2C2O4(具有还原性)溶液混合,用反应中溶液紫色消失快慢的方法研究形响化学反应速率的因素。实验中酸性KMnO4溶液(0.0010mol/L)、H2C2O4溶液的用量均为4mL(忽略加入固体,溶液混合时体积的变化)。
①该反应中氧化剂与还原剂的物质的量之比为________。
②请帮助他们完成以下实验设计表:填写IV中的数据,并将实验目的补充完整。
实验编号 | 温度/K | 催化剂的用量/g | H2C2O4溶液的浓度/mol.L-1 | 实验目的 |
I | 298 | 0.5 | 0.010 | A.实验I和II探究____对反应速率的影响 B.实验I和III探究____对反应速率的影响 C.实验I和IV探究催化剂对反应速率的影响 |
II | 298 | 0.5 | 0.050 | |
III | 323 | 0.5 | 0.010 | |
IV | ____ | ____ | ____ |
③该小组同学对实验II进行了3次实验,测得以下数据:
实验编号 | 溶液退色所需时问t/min | ||
第1次 | 第2次 | 第3次 | |
II | 4.9 | 5.1 | 5.0 |
实验II中用KMnO4表示该反应的平均反应速率为____。