题目内容
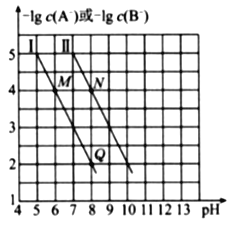
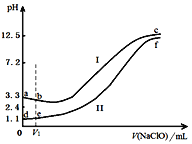
【题目】向两份等体积、等浓度,pH不同的FeSO4溶液中逐滴加入NaClO溶液,实验测得溶液pH随加入NaClO溶液体积变化曲线如下图,实验现象如下表。下列说法不正确的是
实验 | 实验现象 |
Ⅰ | 滴入V1mL NaClO溶液产生大量红褐色沉淀 |
Ⅱ | 滴入V1mL NaClO溶液,溶液变黄,未见沉淀,继续滴加出现红褐色沉淀 |
A. a~b段主要反应的离子方程式为:2Fe2+ + ClO-+5H2O===2Fe(OH)3↓+Cl-+4H+
B. d~e段主要反应的离子方程式为:2Fe2++2ClO-+3H+=== HClO + Cl-+ 2Fe3+ + H2O
C. c、f点pH接近的主要原因是:ClO-+ H2O![]() HClO + OH-
HClO + OH-
D. 向c点溶液中加入过量的浓盐酸,沉淀溶解并有刺激性气味的气体放出
【答案】B
【解析】
A.由实验Ⅰ的现象可知,次氯酸钠与硫酸亚铁反应生成红褐色的沉淀氢氧化铁,根据化合价升降法、电荷守恒和质量守恒可得ab段反应的离子方程式为:2Fe2++ ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+,故A正确;
B.由实验Ⅱ的现象可知,de段有铁离子生成,说明次氯酸根离子将亚铁离子氧化为铁离子,根据化合价升降法、电荷守恒和质量守恒可得de段反应的离子方程式为:2Fe2++ClO-+2H+=Cl-+2Fe3+ +H2O,故B错误;
C.c、f两点的溶质都为氯化钠和过量的次氯酸钠,次氯酸钠为强碱弱酸盐,水解使溶液呈碱性,离子方程式为:ClO-+H2O![]() HClO+OH-,故C正确;
HClO+OH-,故C正确;
D.盐酸可与氢氧化铁反应酸碱中和反应,所以沉淀溶解,在酸性条件下,氯离子与次氯酸根离子发生氧化还原反应生成氯气,氯气具有刺激性的气味,故D正确。
故选B。

练习册系列答案
相关题目