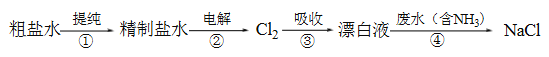��Ŀ����
����Ŀ���мס��ҡ��������������ֶ�����Ԫ�أ�ԭ���������������䳣�����ϼ�����Ϊ+1��-2��+1��+3��-1�������γɵ����ʼ��ת����ϵ����ͼ��ʾ���������ö��Ե缫��⣨�������ӽ���Ĥ��1L l mol/L��A��Һ��
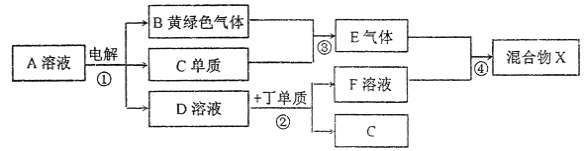
�밴Ҫ��ش��������⣺
��1����Ԫ�����Ԫ��ͬ���壬�ȱ�ԭ�Ӷ�2�����Ӳ㣬��ԭ������Ϊ______���Ʋ���ͬ�����±��������ʷֱ���ˮ��Ӧ���ҳ̶ȵ�������_________��
��2���ס��ҡ��찴ԭ�������1��1��1�γɵĻ�����Y����Ư���ԣ������ʽΪ______��
��3����ͼת����ϵ�в�����������ԭ��Ӧ���У����ţ�______��
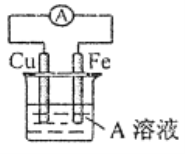
��4����ͨ��ͼ��·Ƭ�̺����ձ��еμ�һ���Լ����ɼ������缫����ʴ���˷�Ӧ�����ӷ���ʽΪ___________��
��5��д����Ӧ�۵Ļ�ѧ����ʽ_________����Ӧ�ڵ����ӷ���ʽΪ___________��
��6������ͼ�и�����Ӧ��Ϊǡ����ȫת����������X�к��е����ʣ���ˮ�⣩��___________��
���𰸡�37 ͬ����Ԫ�صĽ�������˵���������Ӷ���ǿ���Ʋ⼺������ˮ��Ӧ�ϱ������� ![]() �� 3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2�� Cl2 + H2
�� 3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2�� Cl2 + H2![]() 2HCl 2A1+2OH-+2H2O=2AlO2-+3H2�� Al(OH)3��NaCl
2HCl 2A1+2OH-+2H2O=2AlO2-+3H2�� Al(OH)3��NaCl
��������
���A����Һ�õ��������ʣ�����ʺ�ˮ�ŵ磬�õ��Ļ���ɫ����BΪCl2������CΪH2�����߷�Ӧ����EΪHCl��DΪ�������+3�ۣ�������D��Һ��Ӧ������������ΪAl��DΪNaOH��FΪNaAlO2��AΪNaCl����ⷴӦΪ2NaCl+2H2O![]() 2NaOH+H2��+Cl2������2Al��2NaOH��2NaAlO2���õ�ƫ��������HCl���ʵ���֮��Ϊ1��1����H2O+HCl+NaAlO2�TNaCl+Al(OH)3������X�к��е�����ΪAl(OH)3��H2O��NaCl�����Ԫ�ػ��ϼ���ԭ��������֪����ΪHԪ�أ���ΪOԪ�أ���ΪNa����ΪAl����ΪCl��
2NaOH+H2��+Cl2������2Al��2NaOH��2NaAlO2���õ�ƫ��������HCl���ʵ���֮��Ϊ1��1����H2O+HCl+NaAlO2�TNaCl+Al(OH)3������X�к��е�����ΪAl(OH)3��H2O��NaCl�����Ԫ�ػ��ϼ���ԭ��������֪����ΪHԪ�أ���ΪOԪ�أ���ΪNa����ΪAl����ΪCl��
���A����Һ�õ��������ʣ�����ʼ�ˮ�Էŵ磬�õ�����ɫ����BΪCl2������CΪH2�����߷�Ӧ����EΪHCl��DΪ�������+3�ۣ�������D��Һ��Ӧ������������ΪAl��DΪNaOH��FΪNaAlO2��AΪNaCl����ⷴӦΪ2NaCl+2H2O![]() 2NaOH+H2��+Cl2������2Al��2NaOH��2NaAlO2���õ�ƫ��������HCl���ʵ���֮��Ϊ1��1����H2O+HCl+NaAlO2�TNaCl+Al (OH)3������X�к��е�����ΪAl (OH)3��H2O��NaCl�����Ԫ�ػ��ϼ���ԭ��������֪����ΪHԪ�أ���ΪOԪ�أ���ΪNa����ΪAl����ΪCl��
2NaOH+H2��+Cl2������2Al��2NaOH��2NaAlO2���õ�ƫ��������HCl���ʵ���֮��Ϊ1��1����H2O+HCl+NaAlO2�TNaCl+Al (OH)3������X�к��е�����ΪAl (OH)3��H2O��NaCl�����Ԫ�ػ��ϼ���ԭ��������֪����ΪHԪ�أ���ΪOԪ�أ���ΪNa����ΪAl����ΪCl��
(1)��Ԫ�����(Na)Ԫ��ͬ���壬�ȱ�ԭ�Ӷ�2�����Ӳ㣬��ԭ������Ϊ11+8+18=37��ͬ����Ԫ�صĽ�������˵���������Ӷ���ǿ���Ʋ⼺������ˮ��Ӧ�ϱ������ң�
(2)�ס��ҡ��찴ԭ�������1:1:1�γɵĻ�����Y����Ư���ԣ�YΪHClO�������ʽΪ��![]() ��
��
(3)��ͼת����ϵ�У���Ӧ�٢ڢ�����������ԭ��Ӧ����Ӧ�ܲ�����������ԭ��Ӧ��
(4)��ͨ��·Ƭ�̺�FeΪ�������������ҺΪ�Ȼ�����Һ������������ʴ����Fe2+���ӣ���K3[Fe(CN)6]���飬����Fe2+�����ӷ���ʽΪ��3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2����
(5)��Ӧ��Ϊ������������ȼ�գ�������Ӧ�Ļ�ѧ����ʽΪCl2 + H2![]() 2HCl��
2HCl��
��Ӧ��ΪAl����NaOH��Һ���������ķ�Ӧ�����ӷ���ʽΪ��2A1+2OH-+2H2O=2AlO2-+3H2����
(6)�ɷ���֪��X�г�ˮ�⺬�е�����ΪAl(OH)3��NaCl��

 �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д� ���¿쳵����������ϵ�д�
���¿쳵����������ϵ�д�����Ŀ�������£����ʵ���֮��Ϊ2��1��SO2��O2�Ļ���������ݻ�Ϊ2 L�ĺ����ܱ������з�����Ӧ��2SO2(g)��O2(g)![]() 2SO3(g)(����ӦΪ���ȷ�Ӧ)��n(SO2)��ʱ��仯��ϵ���±���
2SO3(g)(����ӦΪ���ȷ�Ӧ)��n(SO2)��ʱ��仯��ϵ���±���
ʱ��/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
����˵����ȷ����( )
A. ��������������ܶȲ���ʱ���÷�Ӧ�ﵽƽ��״̬
B. �÷�Ӧ���е���3����ʱ���淴Ӧ����С������Ӧ����
C. �ӷ�Ӧ��ʼ���ﵽƽ�⣬��SO3��ʾ��ƽ����Ӧ����Ϊ0.01 mol/(L��min)
D. �����ڴﵽƽ��״̬ʱ��ѹǿ����ʼʱ��ѹǿ֮��Ϊ5��4
����Ŀ�������ݵ��������Ũ�ȣ�pH��ͬ��FeSO4��Һ����μ���NaClO��Һ��ʵ������ҺpH�����NaClO��Һ����仯��������ͼ��ʵ���������±�������˵������ȷ����
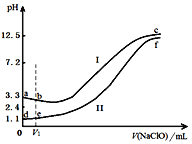
ʵ�� | ʵ������ |
�� | ����V1mL NaClO��Һ�����������ɫ���� |
�� | ����V1mL NaClO��Һ����Һ��ƣ�δ�������������μӳ��ֺ��ɫ���� |
A. a~b����Ҫ��Ӧ�����ӷ���ʽΪ��2Fe2+ + ClO��+5H2O===2Fe(OH)3��+Cl��+4H+
B. d~e����Ҫ��Ӧ�����ӷ���ʽΪ��2Fe2++2ClO��+3H+=== HClO + Cl��+ 2Fe3+ + H2O
C. c��f��pH�ӽ�����Ҫԭ���ǣ�ClO��+ H2O![]() HClO + OH��
HClO + OH��
D. ��c����Һ�м��������Ũ���ᣬ�����ܽⲢ�д̼�����ζ������ų�