题目内容
15.与I2<Br2<Cl2<F2的变化规律(由弱到强或由低到高或由少到多)不符合的是( )| A. | 与氢气反应的难易程度 | B. | 氢化物的熔沸点 | ||
| C. | 非金属性的强弱 | D. | 氢化物稳定性 |
分析 I2<Br2<Cl2<F2的变化规律由F、Cl、Br、I的非金属性决定,结合元素周期律来解答.
解答 解:A.非金属性I<Br<Cl<F,则与氢气反应的难易程度为由难到易,与上述规律一致,故A不选;
B.氢化物的熔沸点与相对分子质量有关,I2、Br2、Cl2、F2的熔沸点由高到低,与上述规律不一致,故B选;
C.非金属性I<Br<Cl<F,与上述规律一致,故C不选;
D.非金属性I<Br<Cl<F,则对应的氢化物稳定性为由弱到强,与上述规律一致,故D不选;
故选B.
点评 本题考查非金属性的比较,为高频考点,把握元素的位置及元素周期律为解答的关键,注意非金属性比较方法及应用,明确氢化物的熔沸点与相对分子质量有关,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
5.除去溴乙烷中的溴单质,最恰当的试剂是( )
| A. | NaOH溶液 | B. | Na2CO3溶液 | C. | NaHSO3溶液 | D. | KI溶液 |
6.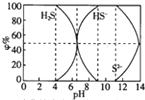 25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )
25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )
 25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )
25℃时0.1mol/L的硫化钠含S组份φ%(以物质的量计算)分布如图如下,下列结论正确的是( )| A. | 当c(HS-)>c(S2-)时,溶液一定显酸性 | |
| B. | 当pH=7时,溶液中有c(Na+)=c(HS-)+2c(S2-)+c(H2S) | |
| C. | 当4<pH时,向其中滴加0.1mol/LCuSO4都有CuS沉淀(Ksp(CuS)=6.3×10-36) | |
| D. | 当pH=9时,溶液中有c(H+)=c(OH-)+c(HS-) |
3.下列说法正确的是( )
| A. | 有H、D、T与16O、17O、18O构成的过氧化氢分子的相对分子质量有36个 | |
| B. | H2、D2、T2互为同素异形体 | |
| C. | H2、D2、T2在相同条件下的密度比为1:2:3 | |
| D. | 氕、氘发生核聚变成其他元素,属于化学变化 |
10.下列表述正确的是( )
| A. | 醛基的结构简式-COH | B. | 聚丙烯的结构简式CH3-CH=CH2 | ||
| C. | 羟基的电子式  | D. | 3-甲基-1-丁烯的键线式 |
4.下列离子或分子在溶液中能大量共存的是( )
| A. | K+.Al3+.Cl-.NO3- | B. | K+.Fe3+.Cl-.SiO32- | ||
| C. | H+.Fe2+.SO42-.Br2 | D. | K+.Ag+.NH3•H2O.NO3- |
5.Co(Ⅲ)的八面体配合物CoClm•nNH3,若1mol 配合物与足量AgNO3溶液作用生成1mol AgCl沉淀,则m、n的值是( )
| A. | m=1,n=5 | B. | m=3,n=4 | C. | m=5,n=1 | D. | m=3,n=3 |
 .
. 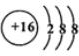 ;D与E能形成一种所有原子最外层均满足8电子的分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.
;D与E能形成一种所有原子最外层均满足8电子的分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.