题目内容
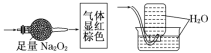
【题目】无色的混合气体甲,可能含NO、CO2、NO2、N2中的几种,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
A.NO2、N2B.NO、CO2
C.NO2、CO2D.NO、CO2、N2
【答案】B
【解析】
二氧化氮是红棕色的气体,所以无色混合气体甲中一定不存在二氧化氮;二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2 ,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有NO、CO2,排水法收集气体,广口瓶被上升的水注满,说明没有N2,所以甲气体的组成为:NO、CO2,故答案为B。

练习册系列答案
相关题目