题目内容
【题目】下表是元素剧期表的一部分,请根据要求填空

(1) 元素②最外层有_____个电子,在化合物中的最低负化合价为________;
(2) 元素⑤形成的离子的结构汞意图为_________;
(3) 用电子式表示元素①和⑦组成的化合物的形成过程:_______________;
(4) 元素④、⑤的最高价氧化物的水化物之间发生反应的离子方程式______________ 。
(5) 下列选项中能证明元素⑦的非金属性强于元素⑥的是________(双选)。
A.H2S的酸性弱于HCl B.S2-的还原性强于C1-
C.H2SO3的酸性强于HClO D.H2S不如HC1稳定
【答案】 6 -2 价 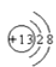
![]() Al(OH)3 + OH- == AlO2- + 2H2O BD
Al(OH)3 + OH- == AlO2- + 2H2O BD
【解析】(1) 元素②是氧,最外层有6个电子,在化合物中的最低负化合价为-2价;(2) 元素⑤形成的Al3+ 离子的结构汞意图为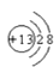 ;(3) 用电子式表示元素①和⑦组成的化合物HCl的形成过程:
;(3) 用电子式表示元素①和⑦组成的化合物HCl的形成过程:![]() ;(4) 元素④、⑤的最高价氧化物的水化物分别为NaOH、Al(OH)3 ,发生反应的离子方程式Al(OH)3 + OH- == AlO2- + 2H2O 。
;(4) 元素④、⑤的最高价氧化物的水化物分别为NaOH、Al(OH)3 ,发生反应的离子方程式Al(OH)3 + OH- == AlO2- + 2H2O 。
(5)能证明元素⑦Cl的非金属性强于元素⑥S的是A. H2S的酸性弱于HCl,不能说明Cl非金属性强,要比较最高价含氧酸的酸性才行,故A错误; B.S2-的还原性强于C1-,Cl2+S2―=S+2Cl―,故B正确;C.H2SO3的酸性强于HClO,不能说明Cl非金属性强,要比较最高价含氧酸的酸性才行,故C错误; D.元素的非金属性越强,形成的气态氢化物就越稳定,H2S不如HC1稳定,故D正确;故选BD。

练习册系列答案
相关题目