题目内容
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:
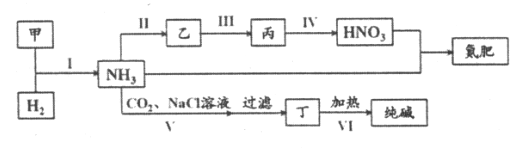
下列说法不正确的是
A. 甲、乙、丙三种物质都含有氮元素 B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用 D. 丁为NaHCO3
【答案】B
【解析】由图可知,甲是氮气,与氢气化合生成氨气。反应Ⅴ是侯氏制碱法,故丁是碳酸氢钠,受热分解生成碳酸钠。氨气发生催化氧化生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,二氧化氮与水反应生成硝酸,硝酸和氨气反应生成硝酸铵,故乙是一氧化氮,丙是二氧化氮,综上所述,甲、乙、丙、丁分别为氮气、一氧化氮、二氧化氮、碳酸氢钠,据此回答问题。
由上述分析可知,甲、乙、丙三种物质中都含有氮元素,A正确;反应Ⅱ为氨气的催化氧化反应,氧化剂为氧气;反应Ⅲ为一氧化氮的氧化,氧化剂为氧气;反应Ⅳ为二氧化氮与水反应生成硝酸和一氧化氮,氧化剂和还原剂均是二氧化氮,B错误;碳酸氢钠分解生成的二氧化碳可以在反应Ⅴ中循环利用,C正确;由上述分析可知,反应Ⅴ为侯氏制碱法,NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl,所以丁为NaHCO3,D正确;正确选项B。

【题目】将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应:2SO2(g)+O2(g)2SO3(g)△H<0.得到如表中的两组数据:
实验编号 | 温度/℃ | 平衡常数/mol﹣1L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
① | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
② | T2 | K2 | 4 | 2 | 0.4 | y | t |
下列说法不正确的是( )
A.x=1.6,y=0.2,t<6
B.T1、T2的关系:T1>T2
C.K1、K2的关系:K2>K1
D.实验1在前6 min的反应速率v (SO2)=0.2 molL﹣1min﹣1
【题目】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
(1)已知:①H2(g)+1/2O2(g)![]() H2O(l) ΔH1=-285.8 kJ/mol;
H2O(l) ΔH1=-285.8 kJ/mol;
②CO (g)+1/2O2 (g)![]() CO2 (g) ΔH2=-283kJ/mol
CO2 (g) ΔH2=-283kJ/mol
③CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
则工业制备甲醇的可逆反应热化学方程式为_______________________________;
(2)恒温恒容条件下,下列描述中能说明上述反应已达平衡状态的是__________。
A.单位时间内生成n mol CO的同时生成2n mol H2 B.ν(H2)正=2ν(CH3OH)逆
C.容器内气体的密度保持不变 D.容器中气体的压强保持不变
(3)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,CO物质的量随时间变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
n(CO)/mol | 1.00 | 0.79 | 0.63 | 0.54 | 0.50 | 0.50 |
则从反应开始到20min时,以ν(H2)=________,该温度下平衡常数K=_______。
(4)加入催化剂后在250 ℃开始反应,CO的平衡转化率与温度、压强的关系如图所示。
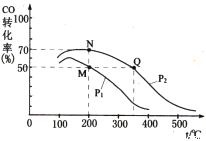
①M、N、Q三点的平衡常数KM、KN、KQ的大小关系为___________________________。
②由M点到N点改变的外界条件是_________。
A、降低温度 B、增大压强
C、改用更好的催化剂 D、通入更多的CO
(5)25℃时以稀硫酸为电解质溶液制成甲醇燃料电池,则负极的电极方程式为_________________________。