题目内容
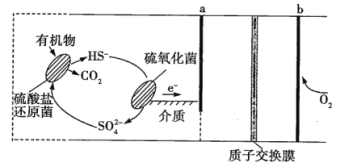
【题目】乙醇(C2H5OH)燃料电池是一种新型电池,其中采用质子(H+)溶剂,在200℃左右时供电,电池总反应为C2H5OH+3O2=2CO2+3H2O,该电池的工作原理如图所示。下列说法正确的是( )
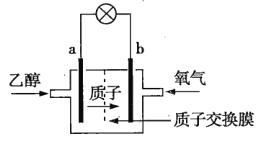
A.通入乙醇的a电极是正极
B..氧气在b电极上发生氧化反应
C.电池工作时,质子向电池的负极迁移
D.电池工作时,电流由b极沿导线流向a极
【答案】D
【解析】
由质子的移动方向可知a为负极,发生氧化反应,b为正极,发生还原反应,据此解答。
A.原电池工作时,阳离子向正极移动,则a为负极,A错误;
B.在b电极上发生反应:O2+4H++4e-=2H2O,氧气得到电子发生还原反应,B错误;
C.电池工作时,阳离子(质子)向电池的正极移动,C错误;
D.电池工作时,电流由正极沿导线流向负极,在该电池中由b极流向a极,D正确。

练习册系列答案
相关题目