题目内容
【题目】H2S在金属离子的鉴定分析、煤化工等领域都有着重要应用。回答下列问题:
I.工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时还生成两种能参与大气循环的氧化物。
(1)该反应的化学方程式为___。
II.H2S可用于检测和沉淀金属阳离子。
(2)由H2S制得的水溶液为氢硫酸,向氢硫酸中滴加少量的硫酸铜溶液,溶液中![]() ___(填“增大”或“减小”)。
___(填“增大”或“减小”)。
(3)已知:25℃时,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27。该温度下,向浓度均为0.1mol·L-1的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=___(溶液体积变化忽略不计)。
III.H2S是煤化工原料气脱硫过程的重要中间体,反应原理如下:
i.COS(g)+H2(g)![]() H2S(g)+CO(g) △H=+7kJ·mol-1;
H2S(g)+CO(g) △H=+7kJ·mol-1;
ii.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-42kJ·mol-1。
CO2(g)+H2(g) △H=-42kJ·mol-1。
(4)已知:断裂1mol分子中的化学键所需吸收的能量如下表所示:

表中x=___。
(5)向10L溶积不变的密闭容器中充入1molCOS(g)、1molH2(g)和1molH2O(g),进行上述两个反应。
①随着温度升高,CO的平衡体积分数___(填“增大”或“减小”),其原因是___。
②T1℃时,测得平衡时体系中COS的物质的量为0.80mol,CO的体积分数为5%。则该温度下,达到平衡时H2的物质的量为___;反应i的平衡常数为___(保留两位有效数字)。
【答案】4SO2+3CH4![]() 4H2S+3CO2+2H2O 减小 8.0×10-3mol/L 1076 增大 反应i为吸热反应,升高温度,化学平衡向正反应方向进行,CO的体积分数增大,反应ii为放热反应,升高温度化学平衡向逆反应方向移动,CO的体积分数也增大 0.85mol 0.044
4H2S+3CO2+2H2O 减小 8.0×10-3mol/L 1076 增大 反应i为吸热反应,升高温度,化学平衡向正反应方向进行,CO的体积分数增大,反应ii为放热反应,升高温度化学平衡向逆反应方向移动,CO的体积分数也增大 0.85mol 0.044
【解析】
I.(1)工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时生成两种能参与大气循环的氧化物,从元素角度考虑,这两种氧化物为CO2和H2O,反应产生H2S;
II.(2)H2S的第一步电离产生H+和HS-,Cu2+与HS-反应生成CuS沉淀和H2S,据此分析判断;
(3)根据溶度积常数计算;
III.(4)根据盖斯定律计算,△H=反应物总键能-生成物总键能;
(5)①根据方程式和图象分析,升高温度,CO的平衡体积分数增大,升高温度使化学反应平衡向吸热方向进行;
②T1℃时,测得平衡时体系中COS的物质的量为0.80mol,此时CO的平衡体积分数为5%,根据方程式计算平衡时H2的物质的量,将各组分平衡浓度代入平衡常数表达式计算反应i的平衡常数。
I.(1)工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时生成两种能参与大气循环的氧化物,从元素角度考虑,这两种氧化物为CO2和H2O,反应产生H2S,则该反应的化学方程式为:4SO2+3CH4![]() 4H2S+3CO2+2H2O,故答案为:4SO2+3CH4
4H2S+3CO2+2H2O,故答案为:4SO2+3CH4![]() 4H2S+3CO2+2H2O;
4H2S+3CO2+2H2O;
II.(2)H2S的第一步电离产生H+和HS-,是不完全电离,Cu2+与HS-反应生成CuS沉淀和H2S,则溶液中![]() 减小,故答案为:减小;
减小,故答案为:减小;
(3)向浓度均为0.1mol/L的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(S2-)= =1.0×10-24mol/L,则溶液中c(Cd2+)=
=1.0×10-24mol/L,则溶液中c(Cd2+)=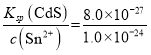 =8.0×10-3mol/L,故答案为:8.0×10-3mol/L;
=8.0×10-3mol/L,故答案为:8.0×10-3mol/L;
III.(4)根据反应i:COS(g)+H2(g)H2S(g)+CO(g)△H=+7kJ/mol,由△H=反应物的总键能-生成物的总键能可得,△H=1319+442-678-x=7,可得x=1076,故答案为:1076;
(5)①根据方程式和图象分析,升高温度,CO的平衡体积分数增大,升高温度使化学反应平衡向吸热方向进行,反应i为吸热反应,升高温度,化学平衡向正反应方向进行,CO的体积分数增大,反应ii为放热反应,升高温度化学平衡向逆反应方向移动,CO的体积分数增大,综合两个反应考虑,CO的体积分数随着温度升高而增大,故答案为:增大;反应i为吸热反应,升高温度,化学平衡向正反应方向进行,CO的体积分数增大,反应ii为放热反应,升高温度化学平衡向逆反应方向移动,CO的体积分数也增大;
②T1℃时,测得平衡时体系中COS的物质的量为0.80mol,此时CO的平衡体积分数为5%,反应起始时,向10L容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),则COS的平衡转化率为α=![]() ×100%=20%,则
×100%=20%,则
反应i的方程式:
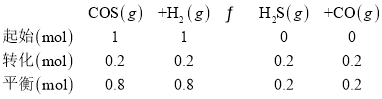
反应ii的方程式:
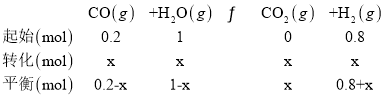
CO的平衡体积分数为5%,则0.2-x=3×5%,可得x=0.05,则平衡时c(COS)=![]() =0.08mol/L,c(H2)=
=0.08mol/L,c(H2)=![]() mol/L=0.085mol/L,n(H2)= 0.085mol/L×10L=0.85mol,因此反应i的化学平衡常数为
mol/L=0.085mol/L,n(H2)= 0.085mol/L×10L=0.85mol,因此反应i的化学平衡常数为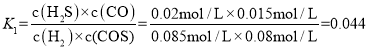
![]() ,故答案为:0.85mol;0.044。
,故答案为:0.85mol;0.044。