题目内容
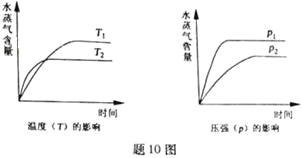
【题目】T℃,将2 mol X和1 mol Y充人一体积为1L。的密闭容器中,已知:2X(g)+Y(g) ![]() 2Z(s) △H=-M kJ·mol-1。10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法正确的是 ( )
2Z(s) △H=-M kJ·mol-1。10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法正确的是 ( )
A. 在10 min时,X的反应速率为0.02 mol·L-1·min-l
B. 在0~10 min内,Y的反应速率为![]() mol·L-1·min-l
mol·L-1·min-l
C. 增加Z的物质的量加快逆反应速率
D. 反应达平衡后,保持T℃,通入稀有气体增加压强,则化学反应速率变快
【答案】B
【解析】A、本题可以求出前10min的平均反应速率,v(X)=0.02 mol·L-1·min-l,但是第10min时的瞬时反应速率无法求解,A错误。B、通过能量变化可得参加反应的Y为N/M mol,所以v(Y)=![]() mol·L-1·min-l,B 正确。C、由于Z是固体,改变Z的量对化学反应速率无影响,C错误。D温度、容器体积不变时,通入稀有气体时,不能改变各气体浓度,所以化学反应速率不改变,D错误。正确答案B。
mol·L-1·min-l,B 正确。C、由于Z是固体,改变Z的量对化学反应速率无影响,C错误。D温度、容器体积不变时,通入稀有气体时,不能改变各气体浓度,所以化学反应速率不改变,D错误。正确答案B。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】碳酸锰(MnCO3)是制造电信器材的软磁铁氧体,也用作脱硫的催化剂,瓷釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是MnO2,还含有Fe2O3、CaCO3、CuO等杂质)制取碳酸锰的流程如下图所示:

已知:还原焙烧主反应为:2MnO2+C![]() 2MnO+CO2↑。
2MnO+CO2↑。
可能用到的数据如下:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Mn(OH)2 |
开始沉淀pH | 1.5 | 6.5 | 4.2 | 8.3 |
沉淀完全pH | 3.7 | 9.7 | 7.4 | 9.8 |
根据要求回答下列问题:
(1)步骤B中若采用质量分数为35%的硫酸(密度ρ=1.26 g/cm3),则其物质的量浓度为____。
(2)步骤C中得到的滤渣主要成分是______________________________,步骤D中还原剂与氧化剂的物质的量之比为_____________________________。
(3)步骤E中调节pH的范围为______________________________。
(4)步骤G的离子方程式为_________________________________________,若Mn2+沉淀完全时测得溶液中CO32-的浓度为2.2×10-6 mol/L,则Ksp(MnCO3)=___________。
(5)实验室可以用Na2S2O8溶液来检验Mn2+是否完全发生反应,原理为:____Mn2+ +____ S2O82- + _____H2O = __________________________________,
①请完成上述离子方程式; _____________
②请描述Mn2+未完全反应时出现的现象__________。
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 验操作和现象 | 实验结论 |
A | 将FeSO4高温灼烧,产生的气体通入盐酸酸化的BaCl2溶液中,产生白色沉淀 | 气体中含有SO3(g) |
B | 向(NH4)2Fe(SO4)2溶液中,滴入新制氯水,后再滴入KSCN溶液,溶液变红 | 原(NH4)2Fe(SO4)2部分或完全被氧化 |
C | 向两支均盛有2mLKI3溶液的试管中分别滴入淀粉溶液和硝酸酸化的AgNO3溶液,前者溶液变蓝色,后者有黄色沉淀 | 原KI3溶液中存在I3- |
D | 向3mL苯中加入1mL液溴,然后加入少量FeBr3充分反应后,产物倒入水中,烧杯底部有褐色油状液体 | 溴苯呈褐色,不溶于水,密度比水大 |
A. A B. B C. C D. D