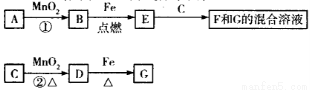
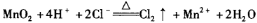题目内容
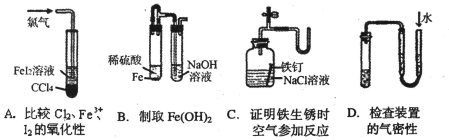
下列装置或操作不能达到 实验目的的是
实验目的的是
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案| A. | $\frac{m}{A+16}$(A-n+8)mol | B. | $\frac{m}{A+16}$(A-n+10)mol | C. | (A-n+2)mol | D. | $\frac{m}{A+16}$(A-n+6)mol |
| A. | 第二周期ⅡA族 | B. | 第三周期ⅡA族 | C. | 第三周期ⅢA族 | D. | 第二周期ⅢA族 |
某化学研究性学习小组拟对一种焰火原料(由两种短周期的常见金属单质组成的合金粉末)进行探究。请完成下列探究报告。
 【探究目的】探究该焰火原料的组成
【探究目的】探究该焰火原料的组成
 【资料检索】①Mg2+检验方法:取2滴待检液,加入2滴2mol·L-1NaOH溶液,再加入1滴镁试剂(Ⅰ)染料(
【资料检索】①Mg2+检验方法:取2滴待检液,加入2滴2mol·L-1NaOH溶液,再加入1滴镁试剂(Ⅰ)染料( 对硝基苯偶氮苯二酚)。若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待检液中含有Mg2+。Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+检出②Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶碱难溶于氯化铵③很多合金是金属互化物,有确定的化学组成
对硝基苯偶氮苯二酚)。若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待检液中含有Mg2+。Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+检出②Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶碱难溶于氯化铵③很多合金是金属互化物,有确定的化学组成
【探究思路】①确定焰火原料所含金属种类;②测定焰火原料的化学式
【实验探究】
(1)甲同学进行了初步试验,实验步骤和实验现象如下。请填写下表。
试验序号 | 实验步骤 | 实验现象 | 结论 |
① | 取少量该焰火原料加入冷水 | 无明显现象 | ________________ |
② | 取少量该焰火原料加入稀盐酸 | 完全溶解,有大量气体 | _________________ |
(2)乙同学取甲第②组实验的溶液,加入镁试剂(Ⅰ)染料,得出合金中不含镁。
乙的结论________________(选填“正确”或“错误”)。判断理由为。
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下。
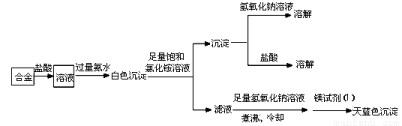
 由丙的实验记录可知,该焰火原料是由_______和_________两种金属组成的合金;实验中滤液加入足量氢氧化钠溶液后需煮沸,煮沸的理由是______________________________。
由丙的实验记录可知,该焰火原料是由_______和_________两种金属组成的合金;实验中滤液加入足量氢氧化钠溶液后需煮沸,煮沸的理由是______________________________。
(4)丁同学利用丙同学的结论,设计如下图所示的实验步骤,确定合金组成。

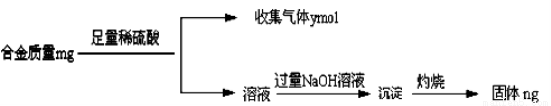
问题讨论:
①能确定合金组成的数据组有______________(填写选项字母);
A.m、n
B.m、y
C.n、y
②若合金中相对原子质量较小的金属的物质的量分数为x,金属总物质的量为7mol,试在下图中作出y随x变化的曲线;

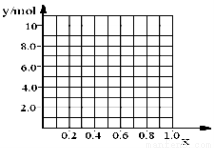
③当y=8.5mol时,该合金是一种金属互化物,其化学式为________________
I.四种制取Cu2O的方法:
a.用炭粉在高温条件下还原CuO制备Cu2O;
b.用葡萄糖还原新制的Cu(OH)2制备Cu2O;
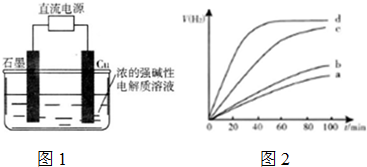
c.电解法制备Cu2O,装置如图1;
d.湿化学法:加热条件下用液态肼(N2H4)还原新制Cu(OH)2
可制备纳米级Cu2O,同时放出N2.
(1)方法c通过阳极氧化制得Cu2O,写出阳极的电极反应式2Cu+2OH--2e-=Cu2O+H2O.
(2)方法d的化学方程式为N2H4+4Cu(OH)2=2Cu2O+N2↑+6H2O,检验纳米Cu2O(粒子大小约几十纳米)已经生成的实验方法是丁达尔效应.
(3)方法d得到的产品中常含有Cu2O称取某产品3.52g(仅含Cu2O和Cu),加入足量的稀硝酸,充分反应后得到标准状况下的NO气体448mL,则产品中Cu2O的质量分数为81.8%.
Ⅱ.用制得的Cu2O进行催化分解水的实验
(4)一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气,发生反应:
2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H═+484KJ•mol-1
不同时段产生O2的物质的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| N(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
(5)用以上四种方法制得的Cu2O在某相同条件下分别对水催化分解,产生氢气的体积V(H2)随时间t变化如图2.
下列叙述正确的是ACD(填字母代号).
A.c、d方法制得的Cu2O催化效率相对较高
B.d方法制得的Cu2O作催化剂时,水的平衡转化率最高
C.催化效果与Cu2O颗粒的粗细、表面活性等有关
D.Cu2O催化水分解时,需要适宜的温度.


 Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如下图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如下图所示,下列叙述正确的是
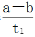 mol·L-1·min-1
mol·L-1·min-1