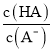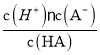题目内容
【题目】由N、B等元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅的制造;由第二周期元素组成的与BCl3互为等电子体的阴离子为_______(填离子符号,填一个)。
(2)氨硼烷(H3N→BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料.
①H3N→BH3中B原子的外围电子排布图_________。
②Ti(BH4)3由TiCl3和LiBH4反应制得,写出该制备反应的化学方程式____;基态Ti3+的成对电子有___对,BH4-的立体构型是____;Ti(BH4)3所含化学键的类型有____;
③氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3;与上述化学方程式有关的叙述不正确的是 _____________
A.氨硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2都是非极性分子
(3)磷化硼(BP)是受到高度关注的耐磨材料,如图1为磷化硼晶胞;
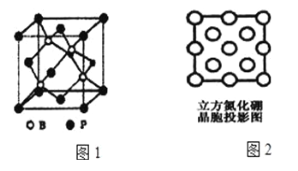
①晶体中P原子填在B原子所围成的____空隙中。
②晶体中B原子周围最近且相等的B原子有____个。
(4)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是__________。图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置______。其中“●”代表B原子,“×”代表N原子。
【答案】NO3-/CO32-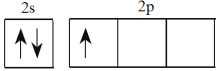 TiCl3+3LiBH4
TiCl3+3LiBH4![]() Ti(BH4)3 + 3LiCl9正四面体配位键、共价键、离子键CD正四面体12氮化硼中硼的原子半径比C大,故其N-B键的键能小于金刚石中的C-C键,所以氮化硼的熔点就越低
Ti(BH4)3 + 3LiCl9正四面体配位键、共价键、离子键CD正四面体12氮化硼中硼的原子半径比C大,故其N-B键的键能小于金刚石中的C-C键,所以氮化硼的熔点就越低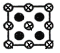
【解析】
(1)根据等电子体原理,原子数相同,价电子数也相同的粒子互为等电子体,所以由第2周期元素组成的与BCl3互为等电子体的阴离子为CO32-或NO3-,故答案为CO32-或NO3-;(2)①B原子的外围电子排布图为![]() ;TiCl3和LiBH4发生复分解反应得到Ti(BH4)3,反应方程式为:TiCl3+3LiBH4
;TiCl3和LiBH4发生复分解反应得到Ti(BH4)3,反应方程式为:TiCl3+3LiBH4![]() Ti(BH4)3 + 3LiCl;基态Ti3+的核外电子排布式为1s22s22p63s23p63d1,故其成对电子数为9;BH4-中B原子的价层电子数为(3+1+4)÷2=4,则其杂化方式为sp3,立体构型为正四面体;BH4-中B原子存在空轨道,与
Ti(BH4)3 + 3LiCl;基态Ti3+的核外电子排布式为1s22s22p63s23p63d1,故其成对电子数为9;BH4-中B原子的价层电子数为(3+1+4)÷2=4,则其杂化方式为sp3,立体构型为正四面体;BH4-中B原子存在空轨道,与
H-能形成配位键,故Ti(BH4)3中所含化学键有离子键、共价键、配位键;③A.氨硼烷N与B间形成的是配位键,故A说法正确;B.在同周期元素中元素的第一电离能随原子序数的增大而增大,而VA族元素的第一电离能要大于相邻元素,则第一电离能:N>O>C>B,故B说法正确;C.反应前CH4中碳原子的轨道杂化类型为sp3,反应后生成的CO2中碳原子的轨道杂化类型为sp;故C说法错误;D.CH4、CO2都是非极性分子,但H2O是极性分子,故D说法错误;答案为CD。(3)①由晶胞结构分析可每个B原子与周围四个P原子成键,同时每个P原子与周围四个B原子成键,P原子位于四个B原子形的正四面体中心,故答案为正四面体;②由晶胞结构可知晶体中B原子周围最近且相等的B原子和P原子周围最近且相等的P原子,以晶胞某个面心的P原子为中心,同一个平面内与之最近且相等的P原子为4个,三个面共12个,故答案为12;(4)氮化硼中硼的原子半径比C大,故其N-B键的键能小于金刚石中的C-C键,所以氮化硼的熔点就越低;立方氮化硼晶胞沿z轴的投影图相当于该晶胞的正视图,其晶胞结构与磷化硼相似,则参照图1可得B与N的相对位置为![]() 。
。

 名校课堂系列答案
名校课堂系列答案【题目】由CO和H2S反应可制得羰基硫(COS)。在恒容的密闭容器中发生反应并达到平衡:CO(g)+H2S(g) ![]() COS(g)+H2(g),数据如下表所示:
COS(g)+H2(g),数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
下列说法正确的是( )
A. 上述反应是吸热反应
B. 实验1达平衡时,CO的转化率为70%
C. 实验2达平衡时,a<7.0
D. 实验3达平平衡后,再充入1.0molH2,平衡逆向移动,平衡常数值增大