题目内容
【题目】下列说法中,不正确的是 ( )。
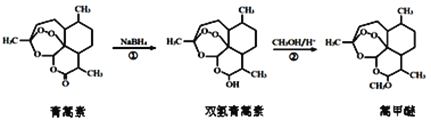
A. 现代药物主要是人工合成的药物
B. 天然药物具有良好的药效,所以不需要进行改造
C. 药物的生物活性跟它的结构中的某些官能团有关
D. 在药物设计领域计算机应用前景广阔
【答案】B
【解析】
结构决定性质,官能团决定物质的特性。

【题目】已知下表为 25℃时某些弱酸的电离平衡常数,依据所给信息判断,下列说法正确的是( )
| HClO |
|
|
|
|
A. 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO— + CO2 + H2O═2HClO + CO32—
B. 相同浓度的CH3COONa和NaClO的混合溶液中,c(CH3COOH) + c(HClO) ═ c(OH—) – c(H+)
C. 25℃时,0.1mol/LCH3COONa溶液中通入CO2至溶液的PH=7时,溶液中:c(Na+) ═ c(CO32—) + c(HCO3—) + c(H2CO3)
D. 向0.1mol/LCH3COONa溶液中加入少量水,溶液中 c(CH3COO—)/c(CH3COOH).c(OH—)增大
【题目】用50 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L 氢氧化钠溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
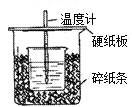
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________;
(2)大烧杯上如不盖硬纸板,求得的中和热数值__________(填“偏大、偏小、无影响”);盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热____________(填“偏大、偏小、无影响”);在中和热测定实验中存在用水洗涤温度计上的盐酸的步骤,若无此操作步骤,则测得的中和热会____________(填“偏大”、“偏小”或“不变”)。
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会____________(填“偏大”、“偏小”或“不变”),其原因是_______________________________________________。
(4)该实验小组做了三次实验,每次取溶液各50 mL,并记录下原始数据(见下表)。
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容c=4.18×10-3kJ/(g·℃),则该反应的中和热为ΔH=_______。根据计算结果,写出该中和反应的热化学方程式______________________。
(5)实验中改用60 mL 1.0 mol·L-1的盐酸跟50 mL 1.1mol·L-1的NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”或“不相等”),所求中和热__________ (填“相等”或“不相等”)。