题目内容
15.下列物质的分类合理的是( )| A. | 碱性氧化物:Na2O、CO、Al2O3、Na2O2 | B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | ||
| C. | 氧化物:Fe2O3、NO、SO2、H2O | D. | 电解质:KNO3、Cl2、HCl、BaSO4 |
分析 氧化物是两种元素组成其中一种是氧元素的化合物;
碱是电离出的阴离子全部是氢氧根的化合物;
碱性氧化物是指能和酸反应生成盐和水的氧化物;
电解质是指在水溶液或熔融状态下能导电的化合物,根据概念来判断.
解答 解:A、CO和算之间不反应,不是碱性氧化物,Al2O3属于两性氧化物,Na2O2和酸反应的产物有盐、水还有氧气,不属于碱性氧化物,故A错误;
B、碳酸钠属于盐类,不属于碱,故B错误;
C、Fe2O3、NO、SO2、H2O是两种元素组成其中一种是氧元素的化合物,属于氧化物,故C正确;
D、氯气是单质,不属于化合物,不属于电解质的范畴,故D错误.
故选C.
点评 本题考查了碱、电解质和碱性氧化物的概念,根据定义来解析是解题关键,难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
5.下列说法正确的是( )
| A. | 某微粒核外电子排布为2、8、8结构,则该微粒一定是氩原子 | |
| B. | 最外层达稳定结构的微粒只能是稀有气体的原子 | |
| C. | F-、Na+、Ca2+、Al3+是与Ne原子具有相同电子层结构的离子 | |
| D. | NH4+与H3O+具有相同的质子数和电子数 |
3.下列说法正确的是( )
| A. | 核磁共振仪、红外光谱仪、质谱仪、紫外光谱仪、元素分析仪、紫外可见分光光度计等都是定性或定量研究物质组成或结构的现代仪器 | |
| B. | 利用元素周期律,人们在过渡元素中寻找各种性能优良的催化剂,使反应的温度降低并提高反应物的转化率,从而起到很好的节能效果 | |
| C. | 淀粉与20%的硫酸混合溶液在沸水浴中充分加热后滴加碘水无蓝色现象,则说明淀粉水解完全 | |
| D. | 分液、蒸馏、渗析、层析及色谱法、钠融法等都是混合体系分离提纯常用的方法 |
10.下列设备工作过程中,将电能转化为化学能的是( )
| A. |  充电器给手机充电 | B. |  太阳能交通信号灯 | ||
| C. |  电饭煲煮饭 | D. |  天然气汽车 |
7.下列说法中,错误的是( )
| A. | 天然气的主要成分是CH4 | |
| B. | 浓硫酸具有吸水性、脱水性、强氧化性 | |
| C. | 淀粉、纤维素、蚕丝、油脂都是高分子化合物 | |
| D. | 工业上采用电解熔化的氧化铝的方法来制备金属铝 |
4.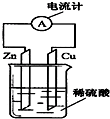 如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )
 如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录:实验后的记录:①Cu为负极,发生氧化反应; ②H+向负极移动; ③Cu电极上有气泡产生;④电子流动方向是Zn→导线→Cu.描述合理的是( )| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
8.短周期元素在周期表中的位置关系如图所示.
(1)X元素的单质的分子式是He,若X核内中子数与质子数相等,则X的摩尔质量为4g/mol.
(2)Y与氢化合形成的化合物的结构式为H-F,在同主族元素的氢化物分子中,该氢化物分子中共价键键能最大,原因是同主族中F原子半径最小,故H-F键长最短,H-F键最稳定,H-F键能最大.
(3)Z单质的晶体属于分子晶体,Z的氢化物的电子式是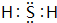 ,该分子中含2个σ键,0个π键(若不含填0).
,该分子中含2个σ键,0个π键(若不含填0).
| X | ||
| Y | ||
| Z |
(2)Y与氢化合形成的化合物的结构式为H-F,在同主族元素的氢化物分子中,该氢化物分子中共价键键能最大,原因是同主族中F原子半径最小,故H-F键长最短,H-F键最稳定,H-F键能最大.
(3)Z单质的晶体属于分子晶体,Z的氢化物的电子式是
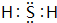 ,该分子中含2个σ键,0个π键(若不含填0).
,该分子中含2个σ键,0个π键(若不含填0).