题目内容
【题目】工业上以Ni的氧化物作催化剂,将丙烯氨氧化制得丙烯腈(CH2=CHCN),然后以H3PO4-K3PO4等作为电解质溶液,电解丙烯腈制已二腈。已知总反应的化学方程式为:4CH2=CHCN+2H2O![]() O2↑+2NC(CH2)4CN。
O2↑+2NC(CH2)4CN。
(1)基态Ni原子价层电子的轨道表达式为_______;在上述总反应的化学方程式中所涉及到的各元素中,电负性由小到大的顺序为_______。
(2)PO43-的空间构型是_______,CH2=CHCN中碳原子的杂化方式为_______ 。
(3)NC(CH2)4CN分子中σ键与π键数目之比为_______。
(4)已知K3PO4是离子晶体,写出其主要物理性质_____(写出2条即可)。
(5)反应中核心元素碳有金刚石、石墨等多种同素异形体。设石墨晶体中碳碳键的键长为am,金刚石晶体中碳碳键的键长为bm,则a____b(填“>”、“=”或“<”),原因________。
(6)金刚石的晶胞结构如下图1所示,已知ZnS晶胞与金刚石晶胞微粒排列方式相同,若图中a为Zn2+,则S2-处于ZnS晶胞中的位置为_________。
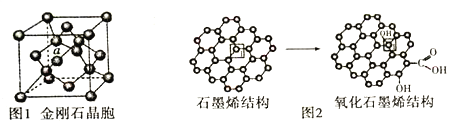
(7)石墨烯中部分碳原子被氧化后,转化为氧化石墨烯(如图2所示)
①石墨烯转化为氧化石墨烯时,1号C与相邻C原子间键能的变化是___(填“变大”、“变小”“不变”)。
②石墨烯具有很大的比表面积,可用于制超级电容器。若石墨烯中碳碳键的键长为am,12g单层石墨烯的单面理论面积约为_______m3(列出计算式即可)。
【答案】 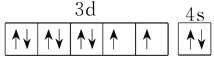 H<C<N<O 正四面体 sp、sp2 15:4 熔融时能导电、熔点较高、硬度较大 < 石墨晶体中碳碳键除σ键外还有大π键,金刚石晶体中碳碳键只有σ键 顶点、面心 变小
H<C<N<O 正四面体 sp、sp2 15:4 熔融时能导电、熔点较高、硬度较大 < 石墨晶体中碳碳键除σ键外还有大π键,金刚石晶体中碳碳键只有σ键 顶点、面心 变小 ![]()
【解析】分析:(1)根据核外电子排布规律书写轨道表达式;非金属性越强,电负性越大;
(2)根据价层电子对互斥理论解答;
(3)根据分子中含有的共价键判断;
(4)根据离子晶体的性质特点解答;
(5)根据石墨和金刚石中含有的化学键分析;
(6)根据金刚石的晶胞结构并依据硫化锌的化学式判断;
(7)石墨烯转化为氧化石墨烯时,1号C 连接的O原子吸引电子能力较强,导致与1号C原子相邻C原子对电子的吸引力减小;根据晶胞结构依据均摊法计算。
详解:(1)Ni的原子序数是28,其基态Ni原子价层电子的轨道表达式为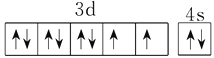 ;非金属性越强,电负性越大,则在上述总反应的化学方程式中所涉及到的各元素中,电负性由小到大的顺序为H<C<N<O。
;非金属性越强,电负性越大,则在上述总反应的化学方程式中所涉及到的各元素中,电负性由小到大的顺序为H<C<N<O。
(2)PO43-的价层电子对数是4,不存在孤对电子,空间构型是正四面体;CH2=CHCN中形成碳碳双键的碳原子是sp2杂化,又因为C与N之间是三键,则该碳原子的杂化方式为sp杂化。
(3)NC(CH2)4CN分子中除C与N之间是三键以外,其余均是单键。由于单键均是σ键,三键中含有1个σ键和2个π键,则σ键与π键数目之比为15:4。
(4)已知K3PO4是离子晶体,其主要物理性质有熔融时能导电、熔点较高、硬度较大等。
(5)由于石墨晶体中碳碳键除σ键外还有大π键,金刚石晶体中碳碳键只有σ键,所以a<b。
(6)已知ZnS晶胞与金刚石晶胞微粒排列方式相同,若图中a为Zn2+,这说明锌全部位于晶胞中,共计是4个,根据化学式ZnS可知S2-处于ZnS晶胞中的位置为顶点、面心。
(7)①石墨烯转化为氧化石墨烯时,1号C 连接的O原子吸引电子能力较强,导致与1号C原子相邻C原子对电子的吸引力减小,所以1号C 与相邻C原子间键能的变化是变小;
②单层石墨烯中含有C原子个数=6×1/3=2,每个六边形面积=![]() 。12g单层石墨烯中原子个数为NA,因此12g单层石墨烯的单面理论面积
。12g单层石墨烯中原子个数为NA,因此12g单层石墨烯的单面理论面积![]() 。
。

 名校课堂系列答案
名校课堂系列答案