题目内容
16.工业上用甲苯为原料生产对羟基苯甲酸乙酯(一种常用的化妆品防腐剂).其生产过程如下图所示(反应条件未全部注明):
请回答下列问题:
(1)有机物A的结构简式为
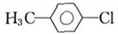 .
.(2)写出反应⑤的化学方程式(注意反应条件):
 +C2H5OH$?_{△}^{浓硫酸}$
+C2H5OH$?_{△}^{浓硫酸}$ +H2O.
+H2O.(3)写出反应②④的反应类型:反应②取代反应、反应④氧化反应.
(4)写出反应③的化学方程式(不必注意反应条件):
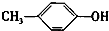 +CH2I→
+CH2I→ +HI.
+HI.(5)在合成路线中,设计③和⑥的目的是保护酚羟基不被氧化.
(6)有机物
 的同分异构体有多种,其中既含有酚羟基又含有酯基的同分异构体共有19种.
的同分异构体有多种,其中既含有酚羟基又含有酯基的同分异构体共有19种.
分析 (1)由于A反应后得到的是对位取代的羟基,所以A的结构为对位取代的氯原子,故A为 ,由
,由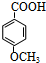 与乙醇发生反应生成B,B再HI作用下生成
与乙醇发生反应生成B,B再HI作用下生成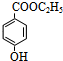 ,故B为
,故B为 ;
;
(2)反应⑤ 与乙醇发生酯化反应生成
与乙醇发生酯化反应生成 ,根据元素守恒写化学方程式;
,根据元素守恒写化学方程式;
(3)反应②为 中氯原子被羟基取代,反应④为
中氯原子被羟基取代,反应④为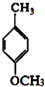 中的甲基被氧化成羧基;
中的甲基被氧化成羧基;
(4)反应③为 与碘甲烷发生取代反应;
与碘甲烷发生取代反应;
(5)在合成路线中,反应③将羟基生成醚键,反应④用强氧化剂将甲基氧化成羧基,反应⑥将醚键生成酚羟基,这样可以达到保护羟基的目的;
(6)根据条件既含有酚羟基又含有酯基可写出 的同分异构体为苯环上连有两个基团为-OH、-COOCH3或-OH、-OOCCH3或-OH、-CH2OOCH,每种结构都有邻间对三种,也可以连三个基团为-OH、-CH3、HCOO-,根据定二动一的原则可知,有10种结构,据此答题.
的同分异构体为苯环上连有两个基团为-OH、-COOCH3或-OH、-OOCCH3或-OH、-CH2OOCH,每种结构都有邻间对三种,也可以连三个基团为-OH、-CH3、HCOO-,根据定二动一的原则可知,有10种结构,据此答题.
解答 解:(1)由于A反应后得到的是对位取代的羟基,所以A的结构为对位取代的氯原子,故A为 ,由
,由 与乙醇发生反应生成B,B再HI作用下生成
与乙醇发生反应生成B,B再HI作用下生成 ,故B为
,故B为 ,故答案为:
,故答案为: ;
;
(2)反应⑤ 与乙醇发生酯化反应生成
与乙醇发生酯化反应生成 ,反应的化学方程式为
,反应的化学方程式为 +C2H5OH$?_{△}^{浓硫酸}$
+C2H5OH$?_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为: +C2H5OH$?_{△}^{浓硫酸}$
+C2H5OH$?_{△}^{浓硫酸}$ +H2O;
+H2O;
(3)反应②为 中氯原子被羟基取代,是取代反应,反应④为
中氯原子被羟基取代,是取代反应,反应④为 中的甲基被氧化成羧基,是氧化反应,
中的甲基被氧化成羧基,是氧化反应,
故答案为:取代反应;氧化反应;
(4)反应③为 与碘甲烷发生取代反应,反应的方程式为
与碘甲烷发生取代反应,反应的方程式为 +CH2I→
+CH2I→ +HI,
+HI,
故答案为: +CH2I→
+CH2I→ +HI;
+HI;
(5)在合成路线中,反应③将羟基生成醚键,反应④用强氧化剂将甲基氧化成羧基,反应⑥将醚键生成酚羟基,酚羟基容易被氧化,所以设计③和⑥的目的是保护酚羟基不被氧化,
故答案为:保护酚羟基不被氧化;
(6)根据条件既含有酚羟基又含有酯基可写出 的同分异构体为苯环上连有两个基团为-OH、-COOCH3或-OH、-OOCCH3或-OH、-CH2OOCH,每种结构都有邻间对三种,也可以连三个基团为-OH、-CH3、HCOO-,根据定二动一的原则可知,有10种结构,所以共有3×3+10=19种,
的同分异构体为苯环上连有两个基团为-OH、-COOCH3或-OH、-OOCCH3或-OH、-CH2OOCH,每种结构都有邻间对三种,也可以连三个基团为-OH、-CH3、HCOO-,根据定二动一的原则可知,有10种结构,所以共有3×3+10=19种,
故答案为:19.
点评 本题考查有机化学推断,难度注定要,题目中有一个隐含条件在推断过程中,即羟基与HI反应生成了甲氧基,此反应反过来也能发生,所以HI起到了能保护羟基的作用.在做此类题目的时候,注意发生反应的官能团以及官能团的位置.

| A. | 一定温度下,向饱和NaOH溶液中加入一小块钠,充分反应后恢复到原来温度,溶液的pH不变,有氢气放出 | |
| B. | 已知钡的活动性处于钾和钠之间,则在溶液中钡离子可氧化金属锌,使之成为锌离子 | |
| C. | 研究小组通过实验探究Cu及其化合物的性质,将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色 | |
| D. | 次氯酸钠是漂粉精的主要成分 |
| A. | 加入有色布条,有色布条褪色,说明溶液中有氯气分子存在 | |
| B. | 溶液呈现黄绿色,且有刺激性气味,说明有氯气分子存在 | |
| C. | 先加入盐酸酸化,再加入硝酸银溶液产生白色沉淀,说明有Cl-存在 | |
| D. | 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
| A. | 原电池的正极和电解池的阴极所发生的反应分别是氧化反应、还原反应 | |
| B. | 温度不变,用惰性电极电解饱和碳酸钠溶液,通电一段时间,溶液的浓度不变,有晶体析出 | |
| C. | 用惰性电极电解CuCl2溶液,一段时间后,要恢复原来的浓度,应加入固体CuSO4 | |
| D. | 以惰性电极电解CuSO4溶液,若阳极上产生的气体的物质的量为0.010mol,则阴极上析出Cu的质量为12.8g |
| A. | 阳极反应为Fe-2e-═Fe2+ | |
| B. | 过程中有Fe(OH)3沉淀生成 | |
| C. | 电路中每转移12mol电子,最多有1molCr2O72-被还原 | |
| D. | 如果石墨做阴阳极,电解过程不变 |
| A. | 摩尔是表示物质质量的单位 | |
| B. | 摩尔是国际七个基本物理量之一 | |
| C. | 用摩尔表示物质的量时,要用化学式指明粒子种类 | |
| D. | 摩尔既是物质的量的单位,又是粒子的数量单位 |
| A. | 用溶解、过滤的方法出去CaO中的CaCO3杂质 | |
| B. | 用结晶法提纯NaCl和KNO3混合物中的KNO3 | |
| C. | 用蒸馏法分离乙醇和乙酸(沸点分别为78℃、118℃)的混合物 | |
| D. | 用萃取和分液的方法可以分离碘和水的混合物 |
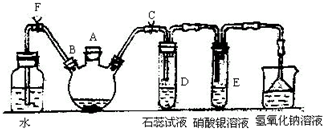 实验室制备溴苯可用如图所示的装置,填写下列空白:
实验室制备溴苯可用如图所示的装置,填写下列空白: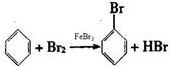 .
.