题目内容
【题目】使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL).
Ⅰ.实验步骤:
(1)配制100mL待测白醋溶液.量取10.00mL食用白醋,注入烧杯中用水稀释后转移到______(填仪器名称)中定容,摇匀即得.
(2)取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴_______作指示剂.
(3)读取盛装0.1000mol/L KOH溶液的_________(填仪器名称)的初始读数.如果液面位置如图所示,则此时的读数为________mL.

(4)滴定:当_______时,停止滴定,并记录KOH溶液的终点读数.重复滴定3次.
Ⅱ.实验记录:
实验数据(mL) 滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(KOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(1)经计算,市售白醋总酸量=______g/100mL.
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是____(填写序号)。
A.碱式滴定管在滴定时未用标准KOH溶液润洗
B.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
C.锥形瓶中加入待测白醋溶液后,再加少量水
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出
【答案】100mL容量瓶 酚酞 碱式滴定管 0.60 溶液由无色恰好变为红色(或浅红色),并在半分钟内不褪色 4.5 ab
【解析】
本题主要考查酸碱中和滴定实验相关知识。Ⅰ.(1)溶液的稀释在烧杯中进行,溶液的定容在对应体积的容量瓶中进行;
(2)强碱滴定弱酸时应选择碱性变色范围内的指示剂酚酞;
(3)根据碱溶液应盛放在碱式滴定管中;根据滴定管的结构与精确度来分析;
(4)滴定终点时溶液颜色发生变化,并在半分钟内不恢复;
Ⅲ.(1)根据数据的合理性求出平均消耗的KOH溶液的体积,然后根据白醋与KOH 溶液反应的关系式来解答;
(2)根据c(待测)=![]() ,分析不当操作对V(标准)以及待测物质的量的影响,以此判断待测液浓度的误差。
,分析不当操作对V(标准)以及待测物质的量的影响,以此判断待测液浓度的误差。
I.(1)量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL容量瓶中定容,摇匀即得待测白醋溶液;
(2)食醋与KOH反应生成了强碱弱酸盐,溶液呈碱性,应选择碱性变色范围内的指示剂酚酞;
(3)KOH 溶液应盛放在碱式滴定管中;滴定管液面的读数0.60mL;
(4)KOH滴定食醋,滴定前溶液为无色,终点时溶液为红色或浅红色,所以滴定的终点为:溶液由无色恰好变为红色或浅红色,并在半分钟内不褪色;
Ⅲ.(1)第1次滴定数据明显偏大,应舍去,其他3次消耗的KOH溶液的体积的平均值为15.00mL;设10mL市售白醋样品含有 CH3COOOH ag,则
CH3COOOH~KOH
60 56
a×0.2 0.1000mol/L×0.015L×56g/mol
解得a=0.450g,样品总酸量![]() =4.5g/100mL,故答案为:4.5;
=4.5g/100mL,故答案为:4.5;
(2)a.碱式滴定管在滴定时未用标准NaOH溶液润洗,标准液浓度降低,造成V(标准)偏大,根据c(待测)=![]() 分析可知c(待测)偏大;
分析可知c(待测)偏大;
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=![]() 分析可知c(待测)偏大;
分析可知c(待测)偏大;
c.锥形瓶中加入待测溶液后,再加少量水,待测白醋中酸的物质的量不变,消耗碱的量不变,根据c(待测)=![]() 分析可知c(待测)不变;
分析可知c(待测)不变;
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出,待测液中醋酸物质的量偏小,造成V(标准)偏小,根据c(待测)=![]() 分析可知c(待测)偏小;综上所述,实验结果偏大的是ab。
分析可知c(待测)偏小;综上所述,实验结果偏大的是ab。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案【题目】乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是礦胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体。乙耽苯胺的制备原理为:

实验参数:
名称 | 相对分子质量 | 性状 | 密度g/cm3 | 沸点/。C | 溶解度 | |
苯胺 | 93 | 无色油状液体,具有还原性 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚等 |
乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水 | 易溶于乙醇、乙醚 |
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。
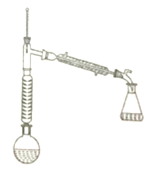
实验步骤:
步骤1:在圆底烧瓶中加入无水苯胺9.30mL,冰醋酸15.4mL,锌粉0.100g,安装仪器,加入沸石,调节加热温度,使分馏柱顶温度控制。在105℃左右,反应约60~80min,反应生成的水及少量醋酸被蒸出。
步骤2:在搅拌下,趁热将烧瓶中的物料以细流状倒入盛有100mL冰水的烧杯中,剧烈搅拌,并冷却,结晶,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步骤3:将此粗乙酰苯胺进行重结晶,晾干,称重,计算产率。
(1)步骤1中所选圆底烧瓶的最佳规格是________。
a. 25ml b. 50ml c. 150ml d. 200ml
(2)实验中加入少量锌粉的目的是_________________________________。
(3)步骤1加热可用____________(填“水浴”、“油浴”或“直接加热”):从化学平衡的角度分析,控制分馏柱上端的温度在105℃左右的原因___________________。
(4)洗涤乙酰苯胺粗品最合适的方法是_______(填序号)。
a.用少量冷水洗 b.用少量热水洗 c.用酒精洗
(5)乙酰苯胺粗品因含杂质而显色,欲用重结品进行提纯,步骤如下
a.蒸发结晶 b.冷却结晶 c.趁热过滤 d.加入活性炭
(6)该实验最终得到纯品9.18g,则乙酰苯胺的产率是_____________%(结果保留一位小数)
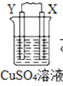
【题目】由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
甲 | 乙 | 丙 | |
装置 |
|
|
|
现象 | 金属W不断溶解 | Y 的质量增加 | W上有气体产生 |
A.四种金属的活动性强弱顺序为Z>W>Y>X
B.装置乙中Y电极上的反应式为Cu2++2e=Cu
C.装置甲中X作原电池正极
D.装置丙中溶液的c(H+)减小